TEORIA DEGLI ENOL E DEGLI ENOLATI
- Dettagli
- Germán Fernández
- TEORIA DEGLI ENOL E DEGLI ENOLATI
- Visite: 37990
Aldeidi e chetoni hanno idrogeni acidi nella posizione vicina del gruppo carbonilico, nota come posizione alfa. Questi idrogeni hanno un pKa compreso tra 18 e 21. 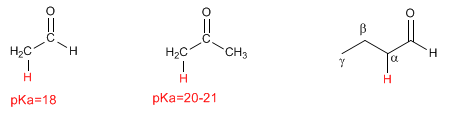
- Dettagli
- Germán Fernández
- TEORIA DEGLI ENOL E DEGLI ENOLATI
- Visite: 32594
Gli enolati agiscono come nucleofili attraverso il carbonio, attaccando un gran numero di elettrofili (aloalcani, epossidi, carbonili, esteri...). A questo punto ci concentreremo sulla reazione tra enlolati e aloalcani, che permette l'aggiunta di catene di carbonio alla posizione a della catena.
Il cicloesanone viene convertito in 2-metilcicloesanone mediante trattamento con LDA seguito da ioduro di metile. 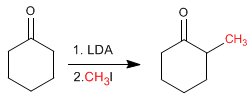
- Dettagli
- Germán Fernández
- TEORIA DEGLI ENOL E DEGLI ENOLATI
- Visite: 21309
Aldeidi e chetoni scambiano i loro idrogeni con deuteri se trattati con DO- /D2O o con D+ /D2O. In mezzi basici la reazione procede attraverso enolati e in mezzi acidi gli intermedi formati sono enoli. 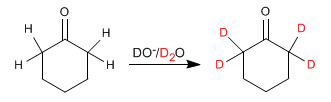
- Dettagli
- Germán Fernández
- TEORIA DEGLI ENOL E DEGLI ENOLATI
- Visite: 56069
Aldeidi e chetoni reagiscono con alogeni in mezzi acidi o basici, producendo la sostituzione di idrogeni per alogeni.
Alogenazione del propanone in ambiente acido: 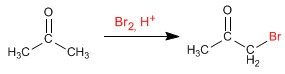
- Dettagli
- Germán Fernández
- TEORIA DEGLI ENOL E DEGLI ENOLATI
- Visite: 105432
Metilchetoni [1] reagisce con alogeni in mezzi basici generando carbossilati [2] e aloformio [3] . 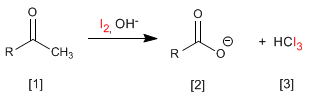
- Dettagli
- Germán Fernández
- TEORIA DEGLI ENOL E DEGLI ENOLATI
- Visite: 118879
Aldeidi e chetoni si condensano in mezzi di base per formare aldoli. Questa reazione è chiamata condensazione aldolica. 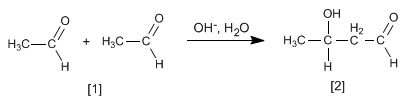
L'aldolo formato si disidrata nel mezzo basico mediante riscaldamento per formare un a , b -insaturo. 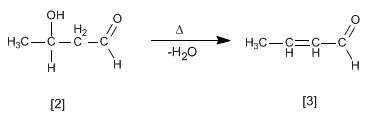
- Dettagli
- Germán Fernández
- TEORIA DEGLI ENOL E DEGLI ENOLATI
- Visite: 53148
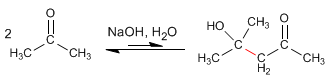
- Dettagli
- Germán Fernández
- TEORIA DEGLI ENOL E DEGLI ENOLATI
- Visite: 48718
Pertanto, il 2,6-eptanedione si condensa con metossido in metanolo per formare 3-metilcicloes-2-enone.
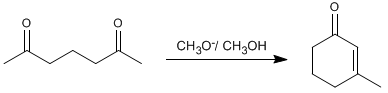
- Dettagli
- Germán Fernández
- TEORIA DEGLI ENOL E DEGLI ENOLATI
- Visite: 80836
La reazione tra due diversi carbonili è chiamata aldolo incrociato o misto. Questa reazione ha utilità sintetica solo in due casi:
1. Solo uno dei carbonili può formare enolati.
2. Uno dei carbonili è molto più reattivo dell'altro.
In tutte le altre situazioni, l'aldolo misto genera miscele di quattro prodotti. Vediamo come esempio la condensazione di etanale e propanale. 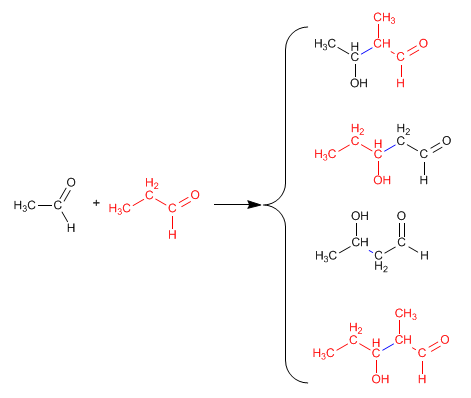
- Dettagli
- Germán Fernández
- TEORIA DEGLI ENOL E DEGLI ENOLATI
- Visite: 72164
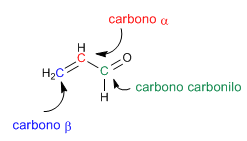 I carbonili a,b -insaturi sono composti organici che hanno un doppio legame tra le posizioni a,b di un'aldeide o di un chetone.
I carbonili a,b -insaturi sono composti organici che hanno un doppio legame tra le posizioni a,b di un'aldeide o di un chetone.
Il propenale o acroleina è un carbonile a,b -insaturo. I suoi due doppi legami coniugati gli conferiscono una reattività speciale.
- Dettagli
- Germán Fernández
- TEORIA DEGLI ENOL E DEGLI ENOLATI
- Visite: 55365
Gli a,b -insaturi sono composti che hanno due posizioni elettrofile: il carbonio carbonilico e il carbonio b .
Addizione 1,2. Gli organometallici del litio attaccano il carbonio carbonilico dando luogo ad addizioni 1,2. 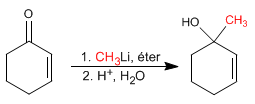
Gli organometallici di litio e magnesio attaccano il carbonio carbonilico degli insaturi a,b
- Dettagli
- Germán Fernández
- TEORIA DEGLI ENOL E DEGLI ENOLATI
- Visite: 53711
Gli enolati di aldeidi o chetoni [1] si aggiungono agli a, b -insaturi [2] per formare 1,5-dicarbonili [3]. Questa reazione è chiamata addizione di Michael. 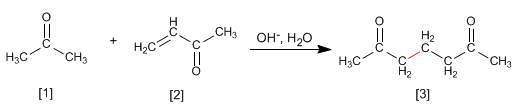
Il propanone reagisce con a, b -insaturo per formare 1,5-dicarbonile
Leggi tutto: Addizione di Michael e annullamento di Robinson