L'acqua è un acido molto debole, con una concentrazione di protoni insufficiente per avviare la reazione di addizione elettrofila. È necessario aggiungere un acido (H2SO4) al mezzo affinché la reazione abbia luogo.
Questa reazione è nota anche come idratazione degli alcheni e genera alcoli.
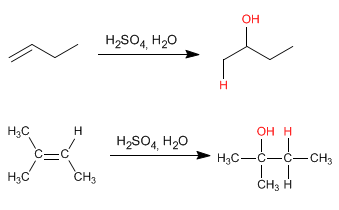
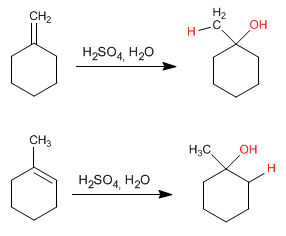
Questa reazione viene condotta con acido solforico diluito 50% solforico/H2O e non richiede idrolisi finale.
Il meccanismo avviene con la formazione di un carbocatione dopo l'aggiunta del protone al doppio legame. L'idratazione degli alcheni è di Markovnikov, cioè il protone si aggiunge al carbonio meno sostituito dell'alchene (carbonio con più idrogeni).
Stadio 1. Attacco dell'alchene al protone (addizione elettrofila)
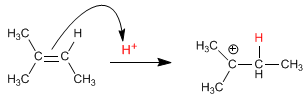
Fase 2. Attacco nucleofilo dell'acqua sul carbocatione formato
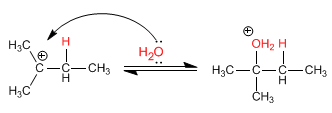
Fase 3. Deprotonazione dell'alcol. L'acqua funge da base.
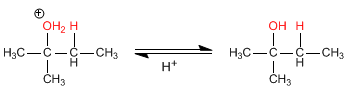
Per il principio di Le Châtelier, all'aumentare della concentrazione di un reagente, l'equilibrio si sposta verso il prodotto finale. Per aumentare la resa di questa reazione si può aggiungere acqua in eccesso, provocando uno spostamento dell'equilibrio verso l'alcool finale.
L'idratazione degli alcheni è una reazione di Markovnikov.