TEORIA DEGLI ALOGENURI ACIDI
- Dettagli
- Germán Fernández
- TEORIA DEGLI ALOGENURI ACIDI
- Visite: 32074
IUPAC nomina gli alogenuri alcanoilici sostituendo l'acido -oico che termina con un numero uguale di atomi di carbonio per -oile . Inoltre, la parola acido è sostituita dal corrispondente alogeno, chiamato sale.
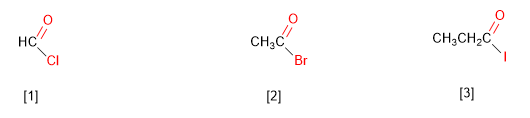
[1] Cloruro di metanoile
[2] Bromuro di etanoile
[3] Ioduro di propanoile
- Dettagli
- Germán Fernández
- TEORIA DEGLI ALOGENURI ACIDI
- Visite: 15824
Gli alogenuri alcanoilici reagiscono con l'acqua a temperatura ambiente per formare acidi carbossilici.
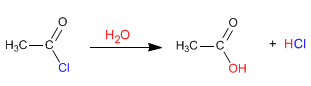
- Dettagli
- Germán Fernández
- TEORIA DEGLI ALOGENURI ACIDI
- Visite: 12878
La reazione degli alogenuri alcanoilici con gli alcoli produce esteri. Gli equilibri di questa reazione sono favoriti eliminando l'acido cloridrico con una base (ammina terziaria, piridina)
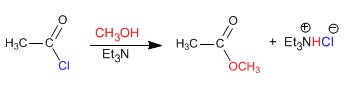
Leggi tutto: Reazione degli alogenuri alcanoilici con gli alcoli
- Dettagli
- Germán Fernández
- TEORIA DEGLI ALOGENURI ACIDI
- Visite: 19237
Le ammine e l'ammoniaca reagiscono con gli alogenuri alcanoilici per formare ammidi. La reazione viene favorita con un eccesso di ammina, in modo da eliminare l'acido cloridrico rilasciato nella reazione.
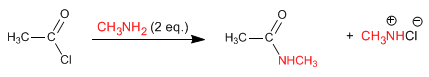
Leggi tutto: Reazione di alogenuri alcanoilici con ammine e ammoniaca
- Dettagli
- Germán Fernández
- TEORIA DEGLI ALOGENURI ACIDI
- Visite: 10524
Gli organometallici di magnesio a -78°C reagiscono con gli alogenuri di alcanoile per formare chetoni. È necessario lavorare a bassa temperatura per evitare di aggiungere un secondo equivalente di organometallico, nel qual caso il prodotto ottenuto sarebbe un alcol.

Leggi tutto: Reazione di alogenuri alcanoilici con organometallici
- Dettagli
- Germán Fernández
- TEORIA DEGLI ALOGENURI ACIDI
- Visite: 17418
Gli alogenuri alcanoilici vengono ridotti ad alcoli con il riducente al litio alluminio
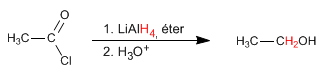
- Dettagli
- Germán Fernández
- TEORIA DEGLI ALOGENURI ACIDI
- Visite: 19440
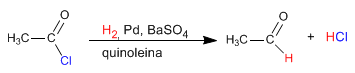
La riduzione degli alogenuri alcanoilici può essere fermata all'aldeide usando idruri modificati. Da litio alluminio idruro si può preparare litio tri(terz-butossi)alluminio idruro. Questo idruro modificato consente la riduzione degli alogenuri acidi ad aldeidi.
Leggi tutto: Riduzione degli alogenuri alcanoilici ad aldeidi
- Dettagli
- Germán Fernández
- TEORIA DEGLI ALOGENURI ACIDI
- Visite: 18701