Nel 1929, il professor S. Kharasch dell'Università di Chicago osservò l'aggiunta anti-Markovnikov di HBr a un alchene dovuta alla presenza di perossidi nel mezzo di reazione.

Il bromo è aggiunto al carbonio meno sostituito dell'alchene, mentre l'idrogeno è legato al carbonio con più sostituenti (antiMarkovnikov)
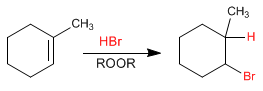
In assenza di perossidi, l'aggiunta di HBr all'alchene è Markovnikov, cioè il bromo si aggiunge al carbonio più sostituito.
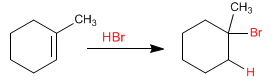
L'addizione di acido bromidrico ad un alchene segue due differenti meccanismi a seconda della presenza o assenza di perossidi nel mezzo di reazione.
In assenza di perossidi, si forma un carbocatione nella posizione più sostituita dell'alchene.
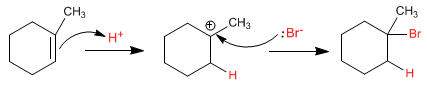
In presenza di perossidi si segue un meccanismo radicalico, con formazione di un intermedio di tipo radicalico sul carbonio più sostituito dell'alchene.
Vediamo il meccanismo della seguente reazione globale:
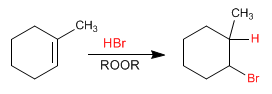
a) Iniziazione
L'iniziazione si compone di due fasi:
Fase 1. Il perossido si dissocia in due radicali alcossilici.
Fase 1. Il perossido si dissocia in due radicali alcossilici.
Fase 2. Astrazione di idrogeno dal bromuro di idrogeno da parte del radicale alcossi, formando radicali di bromo che passano allo stadio di propagazione.
b) Propagazione
La propagazione consiste in due fasi:
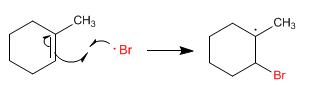
Fase 3. Il radicale bromo viene aggiunto all'alchene.
Fase 4. Il radicale formato sul carbonio estrae idrogeno dal bromuro di idrogeno, formando nuovi radicali di bromo.
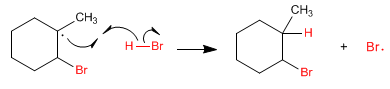
Questa aggiunta è anti-Markovnikov poiché il radicale formato nel passaggio 3 è terziario (altamente stabilizzato dall'iperconiugazione). Un'aggiunta di Markovnikov genererebbe un radicale secondario molto più instabile.