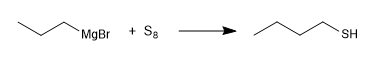I tioli sono caratterizzati dal contenere il gruppo funzionale -SH. Sono denominati terminando il nome della catena principale in -thiol, analogo agli alcoli la cui desinenza è -ol
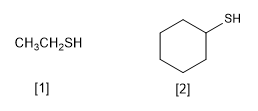
[1] Etantiolo
[2] Cicloesantiolo
I tioli hanno un'acidità maggiore rispetto agli alcoli a causa delle maggiori dimensioni dello zolfo rispetto all'ossigeno. I valori di pKa sono intorno a 10-11, rispetto agli alcoli che hanno valori tra 16-18.
Tuttavia, la maggiore dimensione dello zolfo favorisce la sua polarizzabilità e di conseguenza la sua nucleofilia. I tioli sono nucleofili molto migliori degli alcoli, la loro nucleofilia è ulteriormente migliorata dalla deprotonazione.
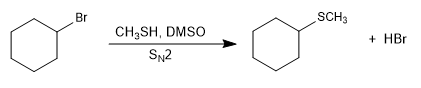
Le reazioni di tipo SN2 diventano più veloci in presenza di un mezzo basico che genera il sale di l-tiolo (tiolato).
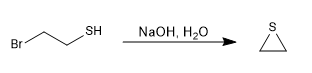
Meccanismo:
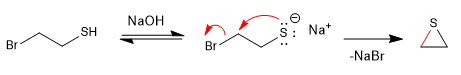
I tioli sono preparati da idrogeno solforato di sodio e un aloalcano primario o secondario.
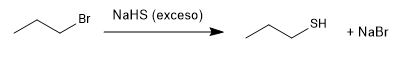
L'eccesso di idrogeno solforato cerca di minimizzare la reazione collaterale per cui il propantiolo riattacca il bromuro di propile per dare un tioetere.
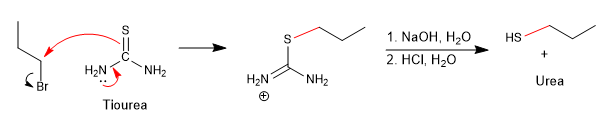
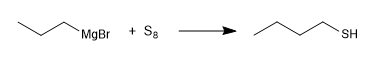
Un modo per evitare questa reazione collaterale è usare la tiourea in combinazione con un aloalcano.

Un altro metodo di sintesi consiste nella reazione del magnesio con lo zolfo elementare.