TEORIA DOS ENÓIS E ENOLATOS
- Detalhes
- Germán Fernández
- TEORIA DOS ENÓIS E ENOLATOS
- Acessos: 39105
- Detalhes
- Germán Fernández
- TEORIA DOS ENÓIS E ENOLATOS
- Acessos: 31830
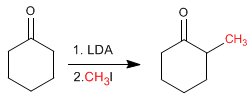
A ciclohexanona é convertida em 2-metilciclohexanona por tratamento com LDA seguido de iodeto de metila.
- Detalhes
- Germán Fernández
- TEORIA DOS ENÓIS E ENOLATOS
- Acessos: 21051
- Detalhes
- Germán Fernández
- TEORIA DOS ENÓIS E ENOLATOS
- Acessos: 54959
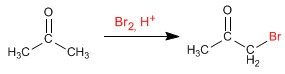
Halogenação de propanona em meio ácido:
- Detalhes
- Germán Fernández
- TEORIA DOS ENÓIS E ENOLATOS
- Acessos: 107243
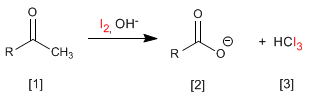
Metilcetonas [1] reagem com halogênios em meios básicos gerando carboxilatos [2] e haloformas [ 3] .
- Detalhes
- Germán Fernández
- TEORIA DOS ENÓIS E ENOLATOS
- Acessos: 114003
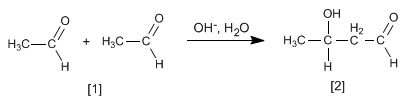
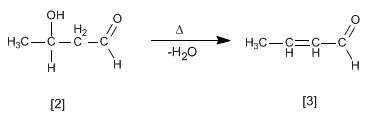
O aldol formado desidrata no meio básico por aquecimento para formar um a , b -insaturado.
- Detalhes
- Germán Fernández
- TEORIA DOS ENÓIS E ENOLATOS
- Acessos: 51007
- Detalhes
- Germán Fernández
- TEORIA DOS ENÓIS E ENOLATOS
- Acessos: 45593
Assim, 2,6-heptanodiona condensa com metóxido em metanol para formar 3-metilciclohex-2-enona.
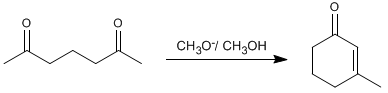
- Detalhes
- Germán Fernández
- TEORIA DOS ENÓIS E ENOLATOS
- Acessos: 78503
A reação entre duas carbonilas diferentes é chamada de aldol cruzado ou misto. Esta reação só tem utilidade sintética em dois casos:
1. Apenas um dos carbonilos pode formar enolatos.
2. Uma das carbonilas é muito mais reativa que a outra.
Em todas as outras situações, o aldol misto gera misturas de quatro produtos. Vejamos como exemplo a condensação de etanal e propanal. 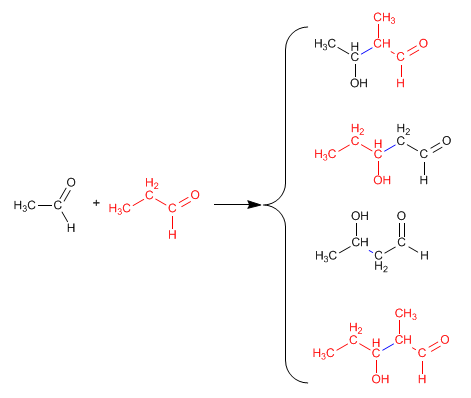
- Detalhes
- Germán Fernández
- TEORIA DOS ENÓIS E ENOLATOS
- Acessos: 66479
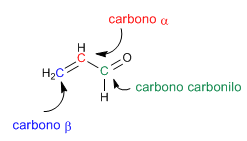 Os carbonilos a,b -insaturados são compostos orgânicos que possuem uma ligação dupla entre as posições a,b de um aldeído ou cetona.
Os carbonilos a,b -insaturados são compostos orgânicos que possuem uma ligação dupla entre as posições a,b de um aldeído ou cetona.
Propenal ou acroleína é um carbonilo a,b -insaturado. Suas duas ligações duplas conjugadas conferem-lhe uma reatividade especial.
- Detalhes
- Germán Fernández
- TEORIA DOS ENÓIS E ENOLATOS
- Acessos: 50057
Os a,b -insaturados são compostos que possuem duas posições eletrofílicas: o carbono carbonílico e o carbono b .
Adições 1,2. Os organometálicos de lítio atacam o carbono carbonílico dando origem a adições 1,2.
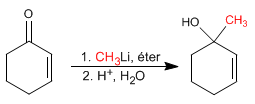
{nota} Os organometálicos do lítio e do magnésio atacam o carbono carbonílico dos a,b -insaturados{/nota}
- Detalhes
- Germán Fernández
- TEORIA DOS ENÓIS E ENOLATOS
- Acessos: 52895
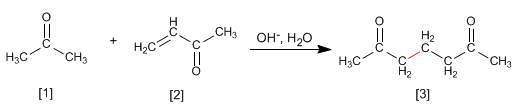
Propanona reage com a,b -insaturado para formar 1,5-dicarbonil