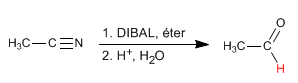TEORIA DEL NITRILE
- Dettagli
- Germán Fernández
- TEORIA DEL NITRILE
- Visite: 42095
IUPAC denomina i nitrili aggiungendo il suffisso -nitrile al nome dell'alcano con lo stesso numero di atomi di carbonio.
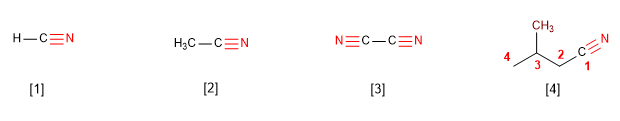
[1] Metanonitrile
[2] Etanonitrile
[3] Etanodinitrile
[4] 3-Metilbutanonitrile
- Dettagli
- Germán Fernández
- TEORIA DEL NITRILE
- Visite: 47244
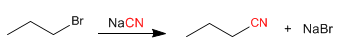
a) Da aloalcani: i nitrili possono essere preparati da aloalcani, mediante processi SN2. La reazione dà buone prestazioni con substrati primari e secondari, quelli terziari vengono preferenzialmente eliminati formando alcheni.
- Dettagli
- Germán Fernández
- TEORIA DEL NITRILE
- Visite: 50406
I nitrili si idrolizzano in ambiente acido, sotto riscaldamento, trasformandosi in acidi carbossilici e sali di ammonio. L'idrolisi dei nitrili è un processo irreversibile.
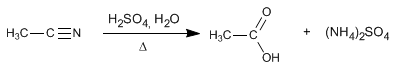
- Dettagli
- Germán Fernández
- TEORIA DEL NITRILE
- Visite: 39026
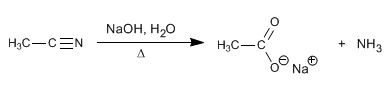
I nitrili vengono idrolizzati con soda acquosa, sotto riscaldamento, per formare carbossilati e ammoniaca.
- Dettagli
- Germán Fernández
- TEORIA DEL NITRILE
- Visite: 26248
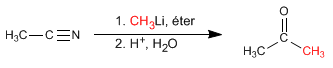
- Dettagli
- Germán Fernández
- TEORIA DEL NITRILE
- Visite: 16790
I nitrili presentano idrogeni a acidi che possono essere rimossi con basi forti, formando enolati di nitrile. Questi idrogeni hanno un pKa di 25.
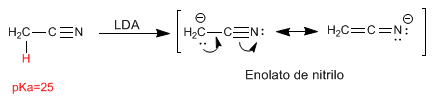
- Dettagli
- Germán Fernández
- TEORIA DEL NITRILE
- Visite: 29031
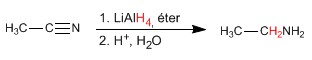
- Dettagli
- Germán Fernández
- TEORIA DEL NITRILE
- Visite: 23970
DIBAL (idruro di diisobutilalluminio) riduce i nitrili ad aldeidi