Le diverse disposizioni spaziali che una molecola può assumere e che vengono interconvertite a temperatura ambiente per rotazione sono chiamate conformazioni.
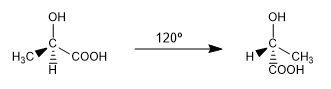
Sono due delle infinite conformazioni che si possono trarre dall'ac. 2-idrossipropanoico. A temperatura ambiente la molecola ruota continuamente attraverso tutte le possibili conformazioni.
Ora diamo un'occhiata alle due conformazioni più caratteristiche dell'etano, le conformazioni alternate ed eclissate.
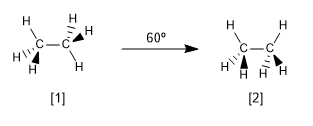
[1] Conformazione alternata dell'etano
[2] Conformazione eclissata dell'etano
Alcune reazioni dipendono fortemente dalla conformazione in cui è disposta la molecola. Pertanto, l'eliminazione E2 richiede che le molecole adottino la disposizione ANTI e la sua velocità dipende dalla concentrazione di molecole che si trovano in questa conformazione.
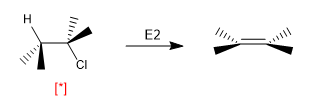
[*] Disposizione "ANTI" H-Cl
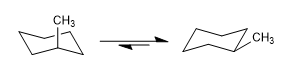
I cicloesani hanno anche due conformazioni a sedia che si interconvertono a temperatura ambiente. La conformazione che lascia più gruppi in posizione equatoriale è solitamente quella con maggiore stabilità.
Un altro esempio di equilibrio conformazionale è rappresentato dai bifenili. Quando entrambi gli anelli sono disposti sullo stesso piano formano un sistema aromatico, ruotando di 90º si rompe la coniugazione tra loro e si rende la molecola più instabile.
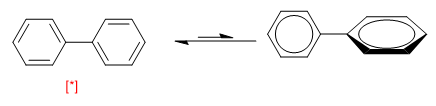
[*] Conformazione più stabile
Tuttavia la presenza di gruppi voluminosi nelle posizioni orto rispetto ad entrambi gli anelli produce repulsioni che costringono la molecola a ruotare, in questo caso la conformazione con gli anelli perpendicolari è più stabile.
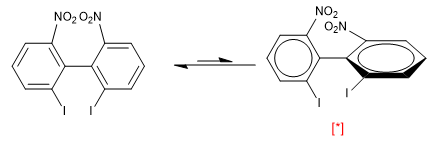
[*] Conformazione più stabile
A temperatura ambiente si osserva solo la conformazione più stabile (lato destro). La repulsione tra i due nitro ei due iodio è così importante che la rotazione del bifenile ha un'energia di attivazione di 19 Kca/mol.
Alcuni collegamenti, anche se apparentemente semplici, non consentono ai gruppi di ruotare liberamente attorno ad essi. I metili DMF danno due singoletti, a diversi spostamenti chimici, nello spettro NMR perché il legame CN ha un forte carattere di doppio legame e limita la rotazione del gruppo.
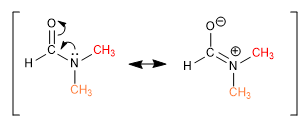
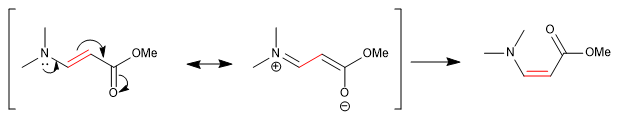
Altri legami, apparentemente doppi, consentono la rotazione grazie al contributo di una struttura risonante in cui si comportano come legami singoli.