REAZIONI DI SOSTITUZIONE (SN1)
- Dettagli
- Germán Fernández
- REAZIONI DI SOSTITUZIONE (SN1)
- Visite: 56640
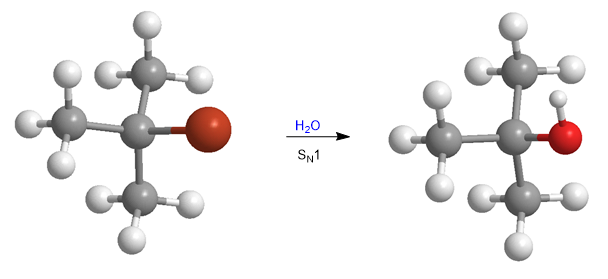
Gli impedimenti sterici rendono i substrati terziari praticamente inerti nei confronti del meccanismo S N 2. Tuttavia, si osserva che questi substrati reagiscono ad una velocità importante con l'acqua, seguendo una cinetica di primo ordine.
Questa osservazione sperimentale implica la proposta di un nuovo meccanismo, chiamato S N 1, che si verifica con substrati terziari e poveri nucleofili, fatti impossibili da spiegare utilizzando il meccanismo S N 2.
- Dettagli
- Germán Fernández
- REAZIONI DI SOSTITUZIONE (SN1)
- Visite: 72264
- Dettagli
- Germán Fernández
- REAZIONI DI SOSTITUZIONE (SN1)
- Visite: 51700
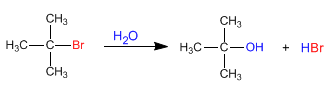
Sia la reazione complessiva:
![]()
Il meccanismo avviene in tre fasi

- Dettagli
- Germán Fernández
- REAZIONI DI SOSTITUZIONE (SN1)
- Visite: 47271
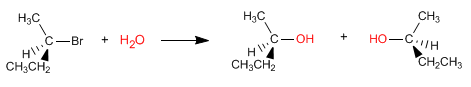
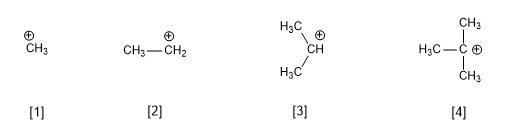
La reazione S N 1 procede attraverso un carbocatione planare, che viene attaccato dal nucleofilo su entrambi i lati, dando origine ad una miscela di stereoisomeri.
- Dettagli
- Germán Fernández
- REAZIONI DI SOSTITUZIONE (SN1)
- Visite: 44619
Il meccanismo S N 1, analogo al meccanismo S N 2, richiede buoni gruppi uscenti.
TsO -> I -> Br -> H 2 O> Cl -
L'acqua non reagisce con il 2-fluoropropano poiché il fluoro è un cattivo gruppo uscente, ma lo fa con il 2-bromopropano.
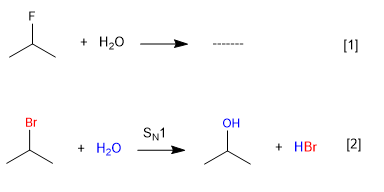
La reazione non ha luogo (gruppo uscente cattivo del fluoro)
- Dettagli
- Germán Fernández
- REAZIONI DI SOSTITUZIONE (SN1)
- Visite: 39008
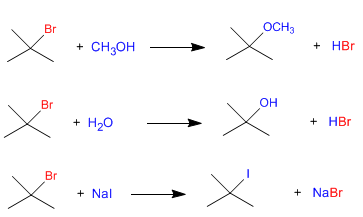
Poiché la fase lenta della sostituzione nucleofila unimolecolare (S N 1) è la dissociazione del substrato e il nucleofilo agisce nella seconda fase, la velocità della reazione non dipende dal nucleofilo. Le seguenti tre reazioni procedono alla stessa velocità poiché partono dallo stesso substrato.
Ovviamente, è necessario che altri fattori, come il solvente, siano gli stessi nelle tre reazioni
- Dettagli
- Germán Fernández
- REAZIONI DI SOSTITUZIONE (SN1)
- Visite: 74520
- Dettagli
- Germán Fernández
- REAZIONI DI SOSTITUZIONE (SN1)
- Visite: 50182