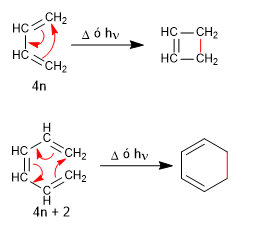
Sia l'1,3-butadiene (4n) che l'1,3,5-esatriene (4n + 2) ciclizzano con luce o calore per dare rispettivamente ciclobutene e 1,3-cicloesadiene.
Come Diels-Alder, le reazioni elettrocicliche sono concertate e stereospecifiche.
Stereochimica delle reazioni elettrocicliche
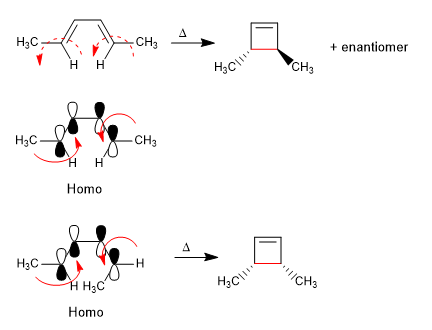
4n sistemi riscaldano il ciclo attraverso l'Homo. La formazione del legame singolo CC presuppone la rotazione degli orbitali nella stessa direzione (conrotatoria).
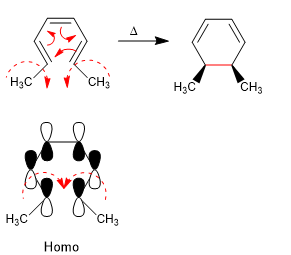
I sistemi 4n + 2 si chiudono con il calore attraverso l'Homo. Lo spin degli orbitali avviene in direzioni opposte (disrotatorio)
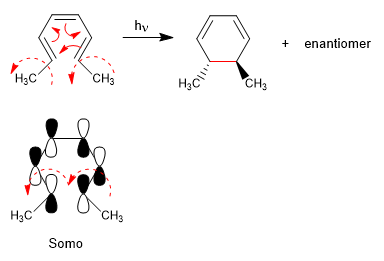
I sistemi 4n con luce si chiudono attraverso il Somo. Lo spin degli orbitali avviene in direzioni opposte (disrotatorio)
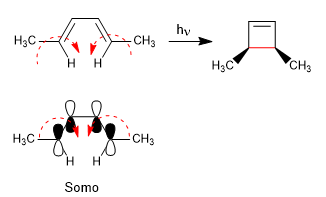
I sistemi 4n + 2 con ciclo di luce attraverso il Somo. La rotazione degli orbitali è nello stesso senso (conrotatorio)