TEORIA DELLA STEREOCHIMICA
- Dettagli
- Germán Fernández
- TEORIA DELLA STEREOCHIMICA
- Visite: 1988
Definizione di isomero
Le molecole che hanno la stessa formula molecolare ma strutture diverse sono chiamate isomeri. È classificato come isomeri strutturali e stereoisomeri.
Isomeri strutturali
Gli isomeri strutturali differiscono nel modo in cui gli atomi sono uniti e sono a loro volta classificati in isomeri di catena posizionali e funzionali.
Stereoisomeri
Gli stereoisomeri hanno tutti i legami identici e si differenziano per la disposizione spaziale dei gruppi. Sono classificati come isomeri cis-trans o geometrici, enantiomeri e diastereoisomeri.
Centro chirale o asimmetrico
Un atomo legato a quattro diversi sostituenti è detto centro chirale o asimmetrico. Una molecola che ha un centro chirale ne ha un'immagine speculare non sovrapponibile, chiamata enantiomero.
Attività ottica
Gli enantiomeri hanno proprietà fisiche quasi tutte identiche, ad eccezione dell'attività ottica. Uno degli enantiomeri ruota la luce polarizzata a destra (destrimano) e l'altro ruota la luce polarizzata a sinistra (mancino).
Stereochimica nelle reazioni
Le reazioni di alogenazione radicalica su molecole in cui si possono formare centri chirali producono miscele di enantiomeri in quantità uguali o di diastereoisomeri in proporzioni diverse.
Separazione degli enantiomeri
Gli enantiomeri hanno quasi tutti le stesse proprietà fisiche, differiscono nella rotazione della luce polarizzata, ma hanno gli stessi punti di fusione e di ebollizione e la stessa solubilità. Pertanto, non possiamo applicare i metodi tradizionali di separazione e dobbiamo ricorrere a tecniche speciali. La separazione tramite diastereoisomeri, consiste nel trasformare la miscela di enantiomeri in una miscela di diastereoisomeri mediante l'aggiunta di un reagente chirale, i diastereoisomeri sono facilmente separabili con metodi fisici.
- Dettagli
- Germán Fernández
- TEORIA DELLA STEREOCHIMICA
- Visite: 110053
La stereochimica è lo studio dei composti organici nello spazio. Per comprendere le proprietà dei composti organici è necessario considerare tutte e tre le dimensioni spaziali. 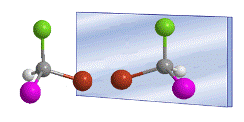 Le basi della stereochimica furono poste da Jacobus van't Hoff e Le Bel, nel 1874. Essi proposero indipendentemente che i quattro sostituenti di un carbonio fossero diretti verso i vertici di un tetraedro, con il carbonio al centro del tetraedro.
Le basi della stereochimica furono poste da Jacobus van't Hoff e Le Bel, nel 1874. Essi proposero indipendentemente che i quattro sostituenti di un carbonio fossero diretti verso i vertici di un tetraedro, con il carbonio al centro del tetraedro.
- Dettagli
- Germán Fernández
- TEORIA DELLA STEREOCHIMICA
- Visite: 292499
Gli isomeri sono molecole che hanno la stessa formula molecolare ma strutture diverse. È classificato come isomeri strutturali e stereoisomeri. Gli isomeri strutturali differiscono nel modo in cui i loro atomi sono legati e sono classificati in isomeri di catena, posizione e funzione. Ad esempio, disegniamo gli isomeri strutturali di formula C2H6O .

[1] Etanolo
[2] Dimetil etere
- Dettagli
- Germán Fernández
- TEORIA DELLA STEREOCHIMICA
- Visite: 265546
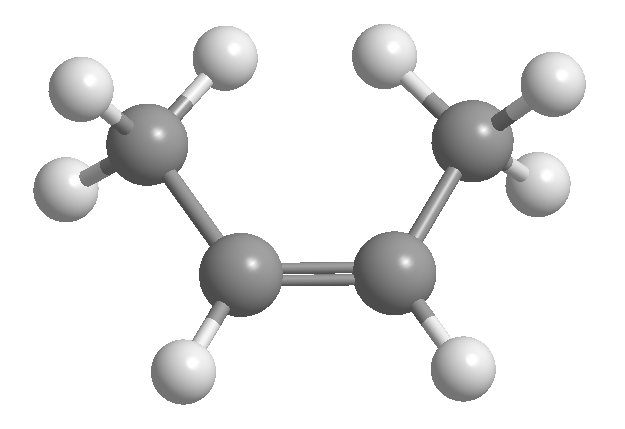
L'isomerismo cis-trans o geometrico è dovuto alla rotazione limitata attorno a un legame carbonio-carbonio. Questa restrizione può essere dovuta alla presenza di doppi legami o cicli. Pertanto, il 2-butene può esistere sotto forma di due isomeri, chiamati cis e trans. L'isomero con gli idrogeni dalla stessa parte si chiama cis, quello con le facce opposte si chiama trans.

[1] cis -2-Butene
[2] trans -2-Butene
- Dettagli
- Germán Fernández
- TEORIA DELLA STEREOCHIMICA
- Visite: 160054
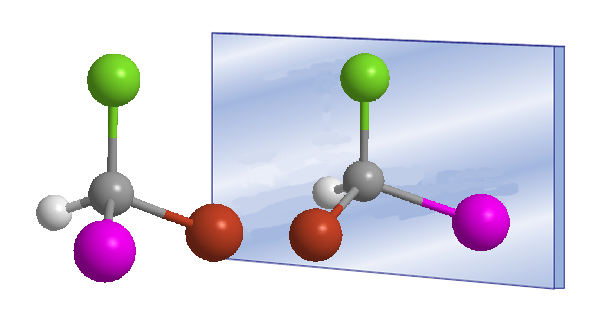
La parola chirale fu introdotta da William Thomson (Lord Kelvin) nel 1894 per designare oggetti non sovrapponibili con la loro immagine speculare. Applicato alla chimica organica, possiamo dire che una molecola è chirale quando essa e la sua immagine speculare non sono sovrapponibili.
- Dettagli
- Germán Fernández
- TEORIA DELLA STEREOCHIMICA
- Visite: 106892
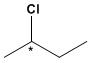 I composti con un carbonio asimmetrico, come il 2-clorobutano, possono esistere come due isomeri.
I composti con un carbonio asimmetrico, come il 2-clorobutano, possono esistere come due isomeri.
- Dettagli
- Germán Fernández
- TEORIA DELLA STEREOCHIMICA
- Visite: 6281
Il numero massimo di stereoisomeri che una molecola presenta può essere calcolato con la formula (2n), dove n rappresenta il numero di atomi di carbonio asimmetrici. Pertanto, una molecola con 2 centri chirali ha 4 stereoisomeri.
Esempio 1. Disegna i possibili stereoisomeri del 2-bromo-3-clorobutano.
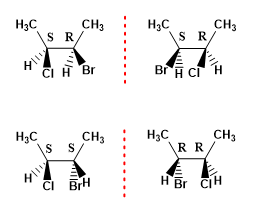
- Dettagli
- Germán Fernández
- TEORIA DELLA STEREOCHIMICA
- Visite: 129551
È necessaria una nomenclatura che distingua gli stereoisomeri di una molecola. Pertanto, nel caso del 2-clorobutano la notazione deve distinguere un enantiomero dall'altro. Cahn, Ingold e Prelog hanno sviluppato alcune regole che ci permettono di distinguere alcuni stereoisomeri da altri, che descrivo di seguito.
- Dettagli
- Germán Fernández
- TEORIA DELLA STEREOCHIMICA
- Visite: 97725
Le molecole che hanno un piano di simmetria o un centro di inversione sono sovrapponibili alla loro immagine speculare. Si dice che siano molecole achirali.
- Dettagli
- Germán Fernández
- TEORIA DELLA STEREOCHIMICA
- Visite: 136110
L'attività ottica è la capacità di una sostanza chirale di ruotare il piano della luce polarizzata. Viene misurato utilizzando un dispositivo chiamato polarimetro.
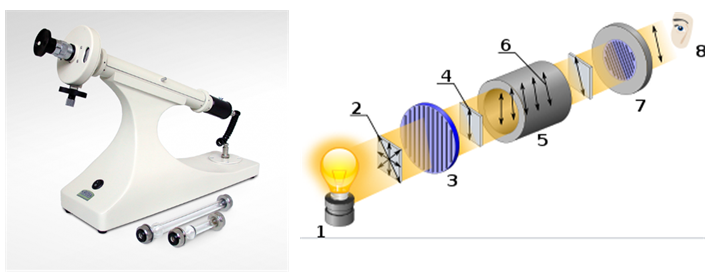
[1] Fonte di luce
[2] Luce non polarizzata
[3] Polarizzatore lineare
[4] Luce polarizzata linearmente
[5] Cuvetta campione
[6] Rotazione in luce polarizzata
[7] Analizzatore
- Dettagli
- Germán Fernández
- TEORIA DELLA STEREOCHIMICA
- Visite: 136884
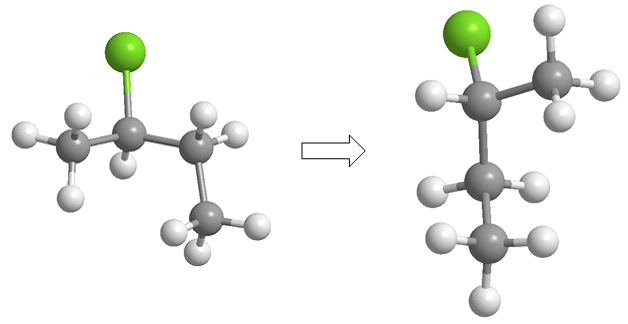
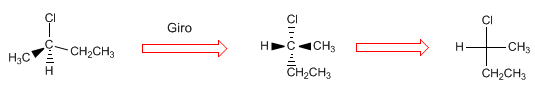
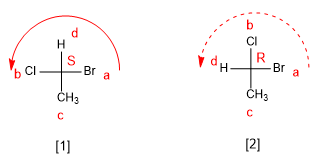
La proiezione consiste nel disegnare una molecola in due dimensioni (piano). Nella proiezione di Fischer la molecola è disegnata a forma di croce con i sostituenti che vanno in fondo al piano in verticale e i gruppi che escono verso di noi in orizzontale, il punto di intersezione di entrambe le rette rappresenta il carbonio proiettato.
- Dettagli
- Germán Fernández
- TEORIA DELLA STEREOCHIMICA
- Visite: 94585
- Dettagli
- Germán Fernández
- TEORIA DELLA STEREOCHIMICA
- Visite: 94044
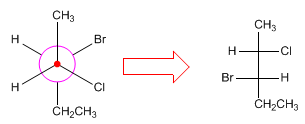
Per convertire le proiezioni di Newman in proiezioni di Fischer, viene disegnata la forma spaziale della molecola, disponendola in una conformazione eclissata per creare la proiezione di Fischer.
- Dettagli
- Germán Fernández
- TEORIA DELLA STEREOCHIMICA
- Visite: 93621
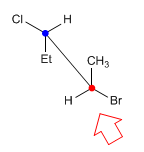 Nella proiezione da cavalletto (detta anche in prospettiva) la linea di osservazione forma un angolo di 45º con il legame carbonio-carbonio. Il carbonio più vicino all'osservatore è in basso ea destra. Mentre quello più lontano è in alto a sinistra.
Nella proiezione da cavalletto (detta anche in prospettiva) la linea di osservazione forma un angolo di 45º con il legame carbonio-carbonio. Il carbonio più vicino all'osservatore è in basso ea destra. Mentre quello più lontano è in alto a sinistra.
- Dettagli
- Germán Fernández
- TEORIA DELLA STEREOCHIMICA
- Visite: 4635
Vedremo come le reazioni chimiche possono introdurre chiralità nelle molecole, ottenendo prodotti sotto forma di miscele racemiche o miscele di diastereoisomeri.
Il butano alogena in presenza di bromo e luce, al carbonio 2, per formare una miscela di enantiomeri. Il radicale formato presenta facce enantiotopiche, che si alogenano con uguale probabilità, dando origine ad una miscela racemica (enantiomeri in uguale proporzione).
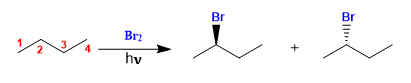
Il meccanismo di questa reazione è costituito da tre fasi: inizio, propagazione e terminazione. La propagazione è il passaggio che determina la stereochimica del prodotto finale.
Alogenazione del butano
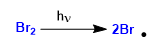
Fase 1. Iniziazione
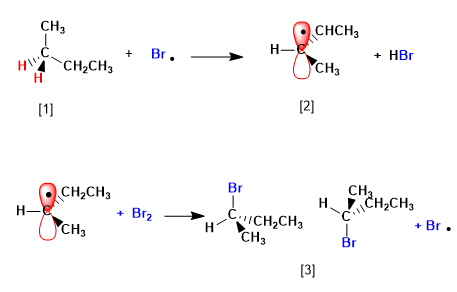
Fase 2. Propagazione
- Dettagli
- Germán Fernández
- TEORIA DELLA STEREOCHIMICA
- Visite: 6545
Reazione stereoselettiva
- Dettagli
- Germán Fernández
- TEORIA DELLA STEREOCHIMICA
- Visite: 4090
Difficoltà nel separare una miscela racemica