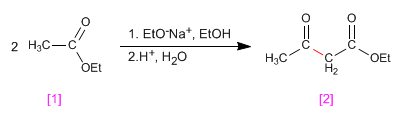TEORIA DOS ÉSTERES
- Detalhes
- Germán Fernández
- TEORIA DOS ÉSTERES
- Acessos: 213763
Os ésteres vêm da condensação de ácidos com álcoois e são nomeados como sais do ácido do qual eles vêm. A nomenclatura IUPAC muda a terminação -óico do ácido para -oato , terminando com o nome do grupo alquila ligado ao oxigênio.
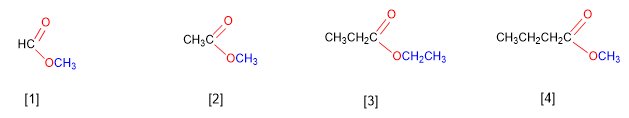
[1] Metanoato de metilo
[2] Etanoato de metilo
[3] Propanoato de etilo
[4] Butanoato de metilo
- Detalhes
- Germán Fernández
- TEORIA DOS ÉSTERES
- Acessos: 105150
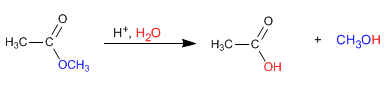
Os ésteres são hidrolisados em meio aquoso, sob catálise ácida ou básica, para formar ácidos carboxílicos e álcoois.
- Detalhes
- Germán Fernández
- TEORIA DOS ÉSTERES
- Acessos: 105906
Os ésteres são hidrolisados em meio aquoso, sob catálise ácida ou básica, para formar ácidos carboxílicos e álcoois. A hidrólise básica é chamada de saponificação e transforma ésteres em carboxilatos.
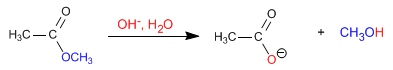
- Detalhes
- Germán Fernández
- TEORIA DOS ÉSTERES
- Acessos: 56749
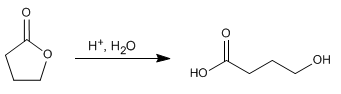
As lactonas são ésteres cíclicos e hidrolisam de maneira análoga aos ésteres não cíclicos, formando compostos contendo grupos ácidos e álcool.
- Detalhes
- Germán Fernández
- TEORIA DOS ÉSTERES
- Acessos: 51764
Os ésteres reagem com álcoois em meio ácido, substituindo seu grupo alcoxi pelo álcool correspondente, como pode ser visto na reação a seguir. Essa reação é chamada de transesterificação.
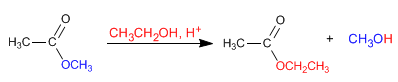
- Detalhes
- Germán Fernández
- TEORIA DOS ÉSTERES
- Acessos: 37510
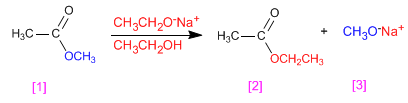
Os ésteres transesterificam na presença de alcóxidos, dependendo da reação:
- Detalhes
- Germán Fernández
- TEORIA DOS ÉSTERES
- Acessos: 37611
- Detalhes
- Germán Fernández
- TEORIA DOS ÉSTERES
- Acessos: 52362
- Detalhes
- Germán Fernández
- TEORIA DOS ÉSTERES
- Acessos: 45459
- Detalhes
- Germán Fernández
- TEORIA DOS ÉSTERES
- Acessos: 27398
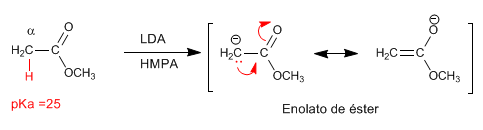
Os ésteres possuem hidrogênios ácidos com pKa=25 em sua posição, que podem ser subtraídos usando bases. A base conjugada é um éster enolato, uma espécie altamente nucleofílica que ataca um número variado de eletrófilos.
- Detalhes
- Germán Fernández
- TEORIA DOS ÉSTERES
- Acessos: 63277
Quando um éster com hidrogênios a é tratado com um equivalente de base (alcóxido) ele se condensa para formar um produto da família dos 3-cetoésteres. Este tipo de reação é conhecido como condensação de Claisen.