1. Éteres de álcoois primários
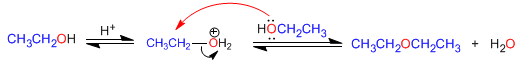
Éteres simétricos podem ser preparados por condensação de álcoois. A reação é realizada sob aquecimento (140°C) e com catálise ácida. Assim, duas moléculas de etanol condensam para formar o éter dietílico.
O mecanismo de reação ocorre nas seguintes etapas:
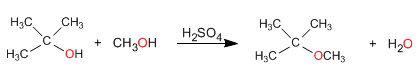
2. Um dos álcoois é secundário ou terciário
Nesse caso, a reação ocorre em condições mais amenas, por meio de mecanismos S N 1 .
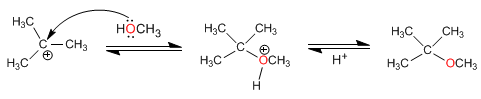
O mecanismo ocorre com a formação de um carbocátion terciário altamente estável
Estágio 1. Protonação do álcool terciário
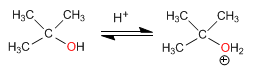
Estágio 2. Formação do carbocátion por perda de água
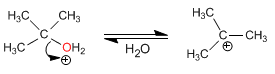
Estágio 3. Ataque nucleofílico do metanol