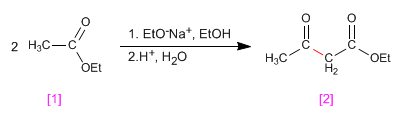ESTER-THEORIE
- Details
- Germán Fernández
- ESTER-THEORIE
- Zugriffe: 220011
Ester stammen aus der Kondensation von Säuren mit Alkoholen und werden als Salze der Säure bezeichnet, aus der sie stammen. Die IUPAC-Nomenklatur ändert die -säure Endung der Säure in -oat und endet mit dem Namen der Alkylgruppe, die an den Sauerstoff gebunden ist.
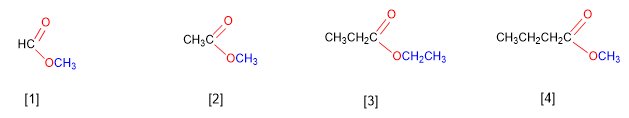
[1] Methylmethanoat
[2] Methylethanoat
[3] Ethylpropanoat
[4] Methylbutanoat
- Details
- Germán Fernández
- ESTER-THEORIE
- Zugriffe: 104854
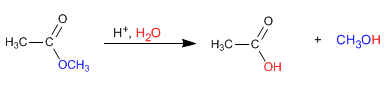
Die Ester werden in wässrigen Medien unter Säure- oder Basenkatalyse zu Carbonsäuren und Alkoholen hydrolysiert.
- Details
- Germán Fernández
- ESTER-THEORIE
- Zugriffe: 106711
Die Ester werden in wässrigen Medien unter Säure- oder Basenkatalyse zu Carbonsäuren und Alkoholen hydrolysiert. Die basische Hydrolyse wird als Verseifung bezeichnet und wandelt Ester in Carboxylate um.
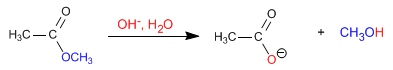
- Details
- Germán Fernández
- ESTER-THEORIE
- Zugriffe: 56774
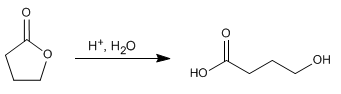
Lactone sind cyclische Ester und hydrolysieren analog zu nichtcyclischen Estern zu säure- und alkoholgruppenhaltigen Verbindungen.
- Details
- Germán Fernández
- ESTER-THEORIE
- Zugriffe: 53600
Ester reagieren mit Alkoholen in sauren Medien, wobei ihre Alkoxygruppe durch den entsprechenden Alkohol ersetzt wird, wie aus der folgenden Reaktion ersichtlich ist. Diese Reaktion wird als Umesterung bezeichnet.
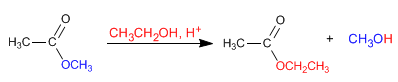
- Details
- Germán Fernández
- ESTER-THEORIE
- Zugriffe: 37957
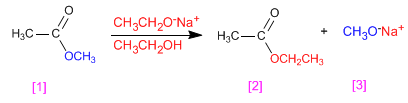
Je nach Reaktion werden Ester in Gegenwart von Alkoholaten umgeestert:
- Details
- Germán Fernández
- ESTER-THEORIE
- Zugriffe: 37846
- Details
- Germán Fernández
- ESTER-THEORIE
- Zugriffe: 55918
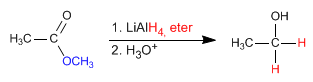
- Details
- Germán Fernández
- ESTER-THEORIE
- Zugriffe: 48014
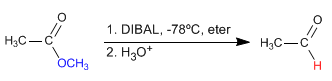
- Details
- Germán Fernández
- ESTER-THEORIE
- Zugriffe: 28305
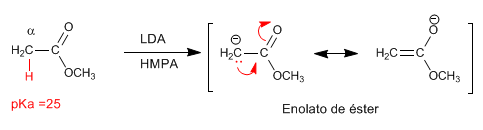
Die Ester haben saure Wasserstoffe mit pKa = 25 in ihrer Position, die mit Basen subtrahiert werden können. Die konjugierte Base ist ein Enolatester, eine hochgradig nucleophile Spezies, die eine unterschiedliche Anzahl von Elektrophilen angreift.
- Details
- Germán Fernández
- ESTER-THEORIE
- Zugriffe: 61764
Wenn ein Ester mit Wasserstoffen a mit einem Äquivalent einer Base (Alkoxid) behandelt wird, kondensiert er, um ein Produkt aus der Familie der 3-Ketoester zu bilden. Diese Art von Reaktion ist als Claisen-Kondensation bekannt.