As aminas têm pontos de fusão e ebulição mais baixos do que os álcoois. Assim, a etilamina ferve a 17ºC, enquanto o ponto de ebulição do etanol é 78ºC.
CH 3 CH 2 OH P.b. = 78ºC
CH 3 CH 2 NH 2 P. eb. = 17ºC
A menor eletronegatividade do nitrogênio, em comparação com a do oxigênio, torna as ligações de hidrogênio formadas pelas aminas mais fracas do que aquelas formadas pelos álcoois.
Observa-se também que as aminas primárias têm pontos de ebulição mais elevados que as secundárias e estas por sua vez mais altas que as terciárias.
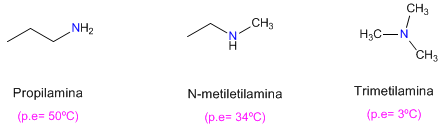
A amina terciária não pode formar pontes de hidrogênio (falta hidrogênio no nitrogênio), o que explica seu baixo ponto de ebulição.
No caso da amina secundária, os impedimentos estéricos devido às cadeias que envolvem o nitrogênio dificultam as interações entre as moléculas.
Aminas com menos de sete carbonos são solúveis em água.