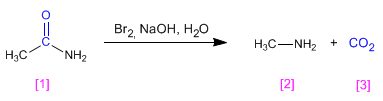TEORIA DAS AMIDAS
- Detalhes
- Germán Fernández
- TEORIA DAS AMIDAS
- Acessos: 117067
Amidas são nomeadas como derivados de ácidos carboxílicos, substituindo a terminação -óico do ácido por -amida .
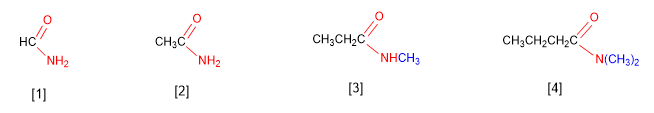
[1] Metanamida
[2] Etanamida
[3] N-Metilpropanamida
[4] N,N-dimetilbutanamida
- Detalhes
- Germán Fernández
- TEORIA DAS AMIDAS
- Acessos: 83895
a) As amidas podem ser obtidas pela reação de aminas com haletos e anidridos de alcanoíla .
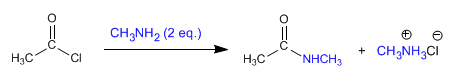
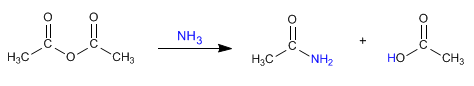
- Detalhes
- Germán Fernández
- TEORIA DAS AMIDAS
- Acessos: 50449
As lactamas são amidas cíclicas obtidas pela condensação, com perda de água, de uma molécula contendo ácido e grupos amino.
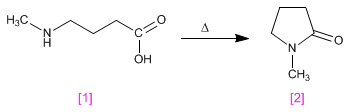
Ácido 4-(aminometil)butanóico [1] condensa sob aquecimento para formar N-metilpirrolidin-2-ona [2] , um solvente aprótico polar.
- Detalhes
- Germán Fernández
- TEORIA DAS AMIDAS
- Acessos: 45681
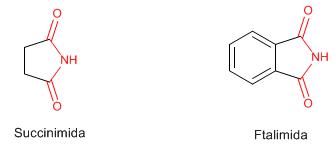
- Detalhes
- Germán Fernández
- TEORIA DAS AMIDAS
- Acessos: 62776
As amidas hidrolisam em meio ácido, sob aquecimento, formando aminas e ácidos carboxílicos. 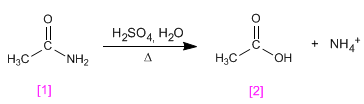
A etanamida [1] é hidrolisada em meio sulfúrico para formar o ácido etanóico [2] .
- Detalhes
- Germán Fernández
- TEORIA DAS AMIDAS
- Acessos: 54437
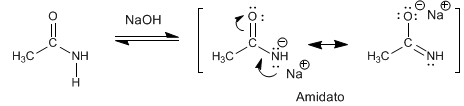
As amidas são transformadas em aminas e ácidos carboxílicos por tratamento com soda aquosa sob aquecimento.
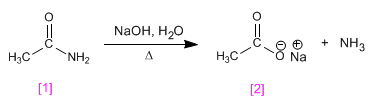
- Detalhes
- Germán Fernández
- TEORIA DAS AMIDAS
- Acessos: 25474
- Detalhes
- Germán Fernández
- TEORIA DAS AMIDAS
- Acessos: 19422
As amidas apresentam hidrogênios ácidos de Pka = 30 no carbono a . A desprotonação da posição a gera uma base estabilizada por ressonância, denominada enolato de amida.
- Detalhes
- Germán Fernández
- TEORIA DAS AMIDAS
- Acessos: 32621
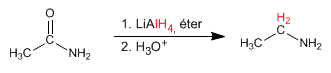
- Detalhes
- Germán Fernández
- TEORIA DAS AMIDAS
- Acessos: 23570
- Detalhes
- Germán Fernández
- TEORIA DAS AMIDAS
- Acessos: 47947
As amidas transformam-se em aminas com um carbono a menos, quando tratadas com bromo em solução básica.