A água é um ácido muito fraco, com concentração de prótons insuficiente para iniciar a reação de adição eletrofílica. É necessário adicionar um ácido (H 2 SO 4 ) ao meio para que a reação ocorra.
Essa reação também é conhecida como hidratação de alcenos e gera álcoois.
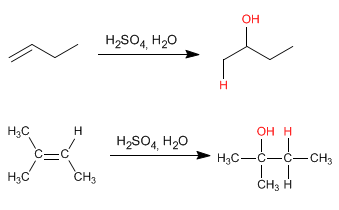
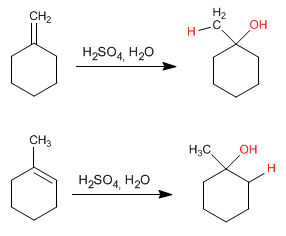
Esta reação é realizada com ácido sulfúrico diluído 50% sulfúrico/H 2 O e não requer hidrólise final.
O mecanismo ocorre com a formação de um carbocátion após a adição do próton à ligação dupla. A hidratação dos alcenos é Markovnikov, ou seja, o próton se soma ao carbono menos substituído do alceno (carbono com mais hidrogênios).
Estágio 1. Ataque do alceno ao próton (adição eletrofílica)
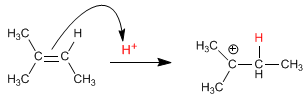
Estágio 2. Ataque nucleofílico da água no carbocátion formado
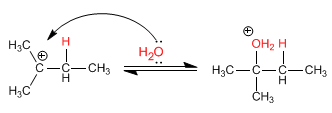
Fase 3. Desprotonação do álcool. A água atua como base.
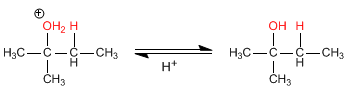
Pelo princípio de Le Châtelier, à medida que a concentração de um reagente aumenta, o equilíbrio se desloca em direção ao produto final. Para aumentar o rendimento dessa reação, pode-se adicionar água em excesso, causando um deslocamento do equilíbrio em direção ao álcool final.
A hidratação de alcenos é uma reação de Markovnikov.