Na natureza, os compostos com ciclos de cinco e seis elos são muito abundantes. No entanto, os ciclos de três e quatro membros aparecem muito raramente em produtos naturais.
Estabilidade em cicloalcanos
Esses fatos experimentais sugerem a maior estabilidade dos ciclos de cinco ou seis membros em relação aos de três ou quatro.
No ano de 1885, o químico alemão Adolf von Baeyer propôs que a instabilidade de pequenos ciclos se devia à tensão dos ângulos de ligação. Os carbonos sp 3 possuem ângulos de ligação natural de 109,5º, no ciclopropano esses ângulos são de 60º, o que é um desvio de 49,5º. Essa deflexão se traduz em estresse, que causa instabilidade na molécula.
O ciclobutano é mais estável, pois seus ângulos de ligação são de 90º e a deflexão é de apenas 19,5º. Baeyer aplicou esse raciocínio aos outros cicloalcanos e previu que o ciclopentano deveria ser mais estável que o ciclohexano.
tensão angular
Observe os ângulos de ligação dos diferentes cicloalcanos:
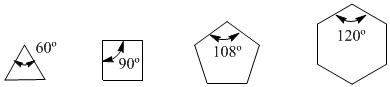
Como o ângulo natural de um carbono sp 3 é de 109,5º, von Baeyer concluiu que o cicloalcano mais estável era o ciclopentano. No entanto, sabemos que Baeyer estava errado, pois o cicloalcano de menor energia (mais estável) é o ciclohexano. O erro de Bayer é assumir que os cicloalcanos são planares e que o único tipo de deformação que eles apresentam é devido aos ângulos de ligação.
Tipos de estresse do anel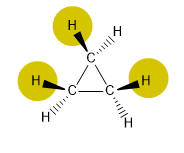
Existem três tipos de estresse que desestabilizam os compostos cíclicos:
1.- Tensão angular de aderência, devido a ângulos que diferem de 109,5º.2.- Tensão eclipsante, devida a átomos ou grupos de átomos próximos, que sofrem repulsões (tensão estérica).
O ciclopropano apresenta uma tensão muito importante, devido aos baixos ângulos de ligação e às interações entre os hidrogênios (eclipsações).