Os halogenetos de hidrogénio adicionam-se aos alcenos, formando os haloalcanos. O próton atua como eletrófilo, sendo atacado pelo alceno no primeiro estágio. HF, HCl, HBr, HI podem ser usados como reagentes nesta reação.
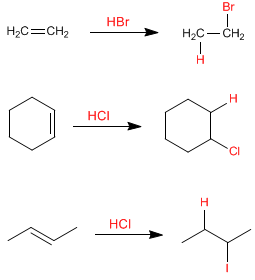
Nestes exemplos, o alceno é simétrico e não importa a qual carbono do alceno o hidrogênio se liga. Em alcenos assimétricos, dois tipos de produtos podem ser dados, dependendo de qual carbono sp 2 o hidrogênio é adicionado. Vejamos um exemplo:
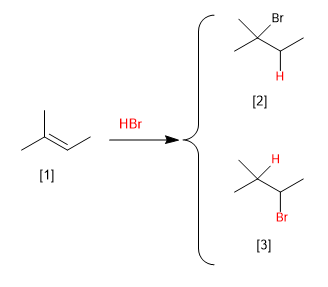
[1] 2-Metil-2-buteno
[2] 2-Bromo-2-metilbutano
[3] 2-Bromo-3-metilbutano (não formado)
A adição de HBr ao 2-metil-2-buteno pode gerar dois produtos, dependendo se o hidrogênio é adicionado ao carbono metil ou ao vizinho. Experimentalmente observa-se que 2-bromo-2-metilbutano é obtido e o 2-bromo-3-metilbutano não aparece como produto da reação.
Como explicar esse fato experimental? A resposta está no mecanismo de reação, que especificaremos a seguir.
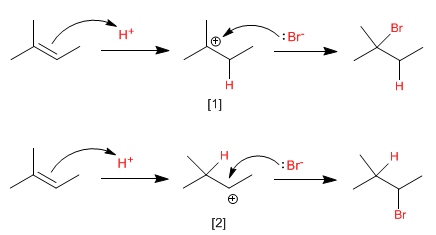
A etapa limitante deste mecanismo é o ataque eletrofílico ao próton (primeira etapa), nesta etapa forma-se um intermediário de reação muito instável, denominado carbocátion.
A maior estabilidade do carbocátion [1] (terciário), em comparação com a do carbocátion [2] (secundário), torna o primeiro mecanismo mais favorável do que o segundo.