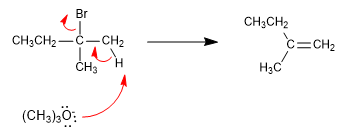
Os alcenos podem ser preparados a partir de haloalcanos e alquilsulfonatos por eliminação bimolecular (E2). No exemplo a seguir, 2-bromo-2-metilbutano reage com metóxido de sódio para formar uma mistura de 2-metil-2-buteno e 2-metil-1-buteno.
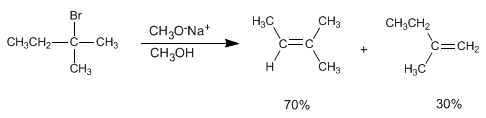
Nesta eliminação, obtém-se o produto mais estável (alceno mais substituído), e diz-se que segue a regra de Saytzev .
O metóxido, base pequena, subtrai o hidrogênio mais interno do haloalcano para produzir o produto mais estável (alceno termodinâmico).
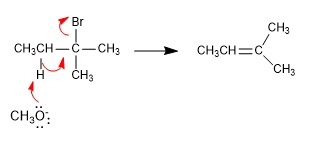
Se usarmos terc-butóxido ou LDA como base, o alceno formado principalmente é 2-metil-1-buteno. As bases impedidas têm dificuldades em acessar o hidrogênio mais interno, subtraindo o hidrogênio mais acessível mais rapidamente, então elas geram o produto menos estável na maior parte. Neste caso a reação é controlada cineticamente e segue a regra de Hofmann .
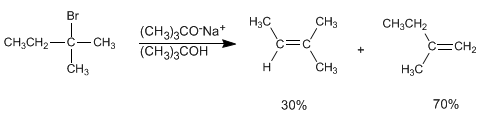
Os hidrogênios localizados nos metils são mais acessíveis ao terc-butóxido do que os hidrogênios mais internos. O alceno formado principalmente é o menos substituído (alceno cinético), e diz-se que a reação segue a regra de Hofmann.