REAKSI SUBSTITUSI (SN1)
- Detail
- Germán Fernández
- REAKSI SUBSTITUSI (SN1)
- Dilihat: 57092
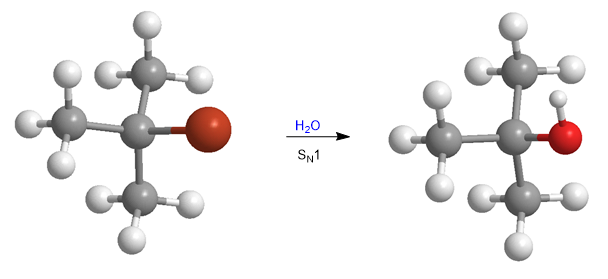
Hambatan sterik membuat substrat tersier praktis inert terhadap mekanisme S N 2. Namun, diamati bahwa substrat ini bereaksi pada laju yang penting dengan air, mengikuti kinetika orde pertama.
Pengamatan eksperimental ini menyiratkan mengusulkan mekanisme baru, yang disebut S N 1, yang terjadi dengan substrat tersier dan nukleofil yang buruk, fakta yang tidak mungkin dijelaskan dengan menggunakan mekanisme S N 2.
- Detail
- Germán Fernández
- REAKSI SUBSTITUSI (SN1)
- Dilihat: 72454
- Detail
- Germán Fernández
- REAKSI SUBSTITUSI (SN1)
- Dilihat: 51643
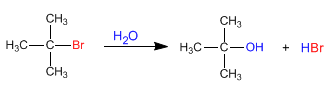
Biarkan reaksi keseluruhan menjadi:
![]()
Mekanismenya terjadi dalam tiga langkah

- Detail
- Germán Fernández
- REAKSI SUBSTITUSI (SN1)
- Dilihat: 47368
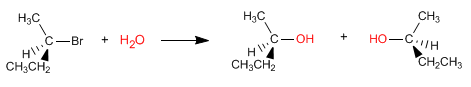
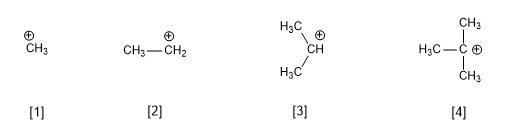
Reaksi S N 1 berlangsung melalui karbokation planar, yang diserang oleh nukleofil di kedua sisi, sehingga menimbulkan campuran stereoisomer.
- Detail
- Germán Fernández
- REAKSI SUBSTITUSI (SN1)
- Dilihat: 44216
Mekanisme S N 1, analog dengan mekanisme S N 2, membutuhkan gugus lepas yang baik.
TsO -> I -> Br -> H 2 O> Cl -
Air tidak bereaksi dengan 2-Fluoropropana karena fluor adalah gugus pergi yang buruk, tetapi bereaksi dengan 2-Bromopropana.
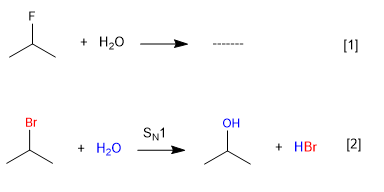
[1 ] Reaksi tidak berlangsung (gugus pergi yang buruk Fluor)
- Detail
- Germán Fernández
- REAKSI SUBSTITUSI (SN1)
- Dilihat: 38643
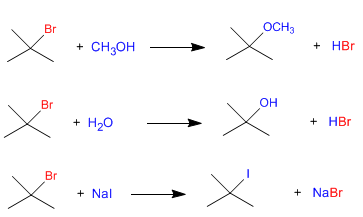
Karena langkah lambat substitusi nukleofilik unimolekuler ( SN 1) adalah disosiasi substrat, dan nukleofil bekerja pada langkah kedua, laju reaksi tidak bergantung pada nukleofil. Tiga reaksi berikut berjalan dengan kecepatan yang sama karena dimulai dari substrat yang sama.
Jelas, faktor-faktor lain, seperti pelarut, harus sama dalam ketiga reaksi
- Detail
- Germán Fernández
- REAKSI SUBSTITUSI (SN1)
- Dilihat: 75667
- Detail
- Germán Fernández
- REAKSI SUBSTITUSI (SN1)
- Dilihat: 49766