RÉACTIONS DE SUBSTITUTION (SN1)
- Détails
- Germán Fernández
- RÉACTIONS DE SUBSTITUTION (SN1)
- Affichages : 57881
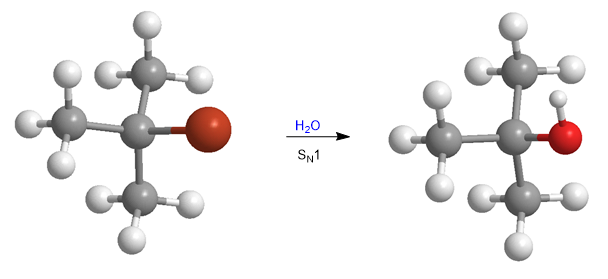
Les encombrements stériques rendent les substrats tertiaires pratiquement inertes vis-à-vis du mécanisme S N 2. Cependant, on observe que ces substrats réagissent à une vitesse importante avec l'eau, suivant une cinétique du premier ordre.
Cette observation expérimentale implique de proposer un nouveau mécanisme, appelé S N 1, qui se produit avec des substrats tertiaires et des nucléophiles pauvres, faits impossibles à expliquer par le mécanisme S N 2 .
- Détails
- Germán Fernández
- RÉACTIONS DE SUBSTITUTION (SN1)
- Affichages : 73331
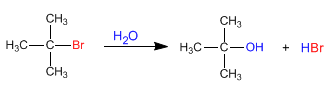
Le S N 1 a un mécanisme étagé. Dans la première étape, le substrat est ionisé par perte du groupe partant, sans que le nucléophile agisse, formant un carbocation. Dans la deuxième étape, le nucléophile attaque le carbocation formé, obtenant le produit final. ![]()
- Détails
- Germán Fernández
- RÉACTIONS DE SUBSTITUTION (SN1)
- Affichages : 52686
Soit la réaction globale :
![]()
Le mécanisme se déroule en trois étapes

- Détails
- Germán Fernández
- RÉACTIONS DE SUBSTITUTION (SN1)
- Affichages : 47485
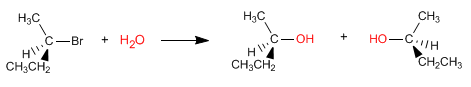
La réaction S N 1 se déroule à travers un carbocation plan, qui est attaqué par le nucléophile des deux côtés, donnant lieu à un mélange de stéréoisomères.
- Détails
- Germán Fernández
- RÉACTIONS DE SUBSTITUTION (SN1)
- Affichages : 44835
Le mécanisme S N 1 , analogue au mécanisme S N 2 , nécessite de bons groupes partants.
TsO -> I -> Br -> H 2 O> Cl -
L'eau ne réagit pas avec le 2-fluoropropane puisque le fluor est un mauvais groupe partant, mais elle le fait avec le 2-bromopropane.
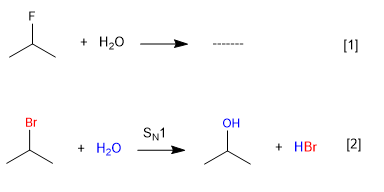
[1 ] La réaction n'a pas lieu (Fuor mauvais groupe partant)
- Détails
- Germán Fernández
- RÉACTIONS DE SUBSTITUTION (SN1)
- Affichages : 39331
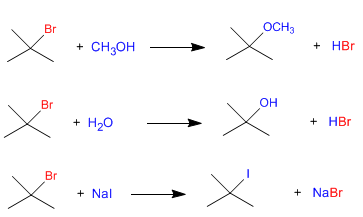
Étant donné que l'étape lente de la substitution nucléophile unimoléculaire (S N 1) est la dissociation du substrat et que le nucléophile agit dans la deuxième étape, la vitesse de la réaction ne dépend pas du nucléophile. Les trois réactions suivantes se déroulent à la même vitesse puisqu'elles partent du même substrat.
Évidemment, il faut que les autres facteurs, comme le solvant, soient les mêmes dans les trois réactions
- Détails
- Germán Fernández
- RÉACTIONS DE SUBSTITUTION (SN1)
- Affichages : 74954
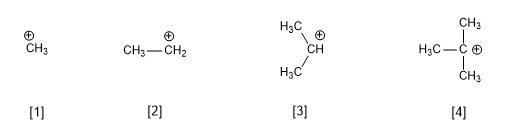
- Détails
- Germán Fernández
- RÉACTIONS DE SUBSTITUTION (SN1)
- Affichages : 50439
Les solvants protiques (eau, alcools) stabilisent les carbocations par interaction entre l'oxygène polarisé négativement du solvant et le carbone positif. Ces interactions diminuent l'énergie d'activation de l'étape lente, favorisant la vitesse de la réaction.