РЕАКЦИИ ЗАМЕЩЕНИЯ (SN1)
- Информация о материале
- Germán Fernández
- РЕАКЦИИ ЗАМЕЩЕНИЯ (SN1)
- Просмотров: 56528
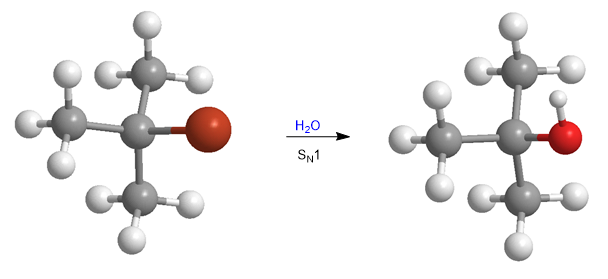
Стерические препятствия делают третичные субстраты практически инертными по отношению к механизму S N 2. Однако наблюдается, что эти субстраты реагируют с водой с большой скоростью, следуя кинетике первого порядка.
Это экспериментальное наблюдение подразумевает предложение нового механизма, названного S N 1, который происходит с третичными субстратами и плохими нуклеофилами, факты, которые невозможно объяснить с помощью механизма S N 2.
- Информация о материале
- Germán Fernández
- РЕАКЦИИ ЗАМЕЩЕНИЯ (SN1)
- Просмотров: 76883
- Информация о материале
- Germán Fernández
- РЕАКЦИИ ЗАМЕЩЕНИЯ (SN1)
- Просмотров: 51151
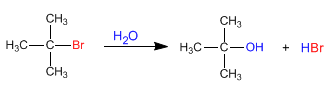
Пусть общая реакция будет:
![]()
Механизм происходит в три этапа

- Информация о материале
- Germán Fernández
- РЕАКЦИИ ЗАМЕЩЕНИЯ (SN1)
- Просмотров: 47032
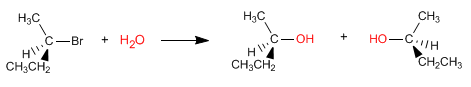
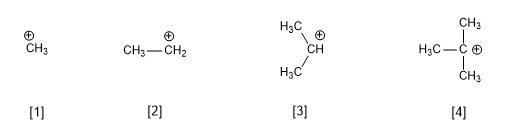
Реакция S N 1 протекает через плоский карбокатион, который атакуется нуклеофилом с обеих сторон, в результате чего образуется смесь стереоизомеров.
- Информация о материале
- Germán Fernández
- РЕАКЦИИ ЗАМЕЩЕНИЯ (SN1)
- Просмотров: 44061
Механизм S N 1, аналогичный механизму S N 2, требует хороших уходящих групп.
ЦО -> I -> Br -> H 2 O> Cl -
Вода не реагирует с 2-фторпропаном, поскольку фтор является плохой уходящей группой, но реагирует с 2-бромпропаном.
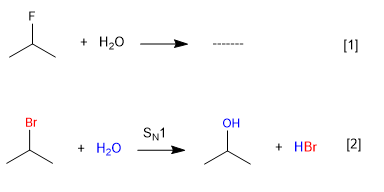
[1 ] Реакция не идет (плохая уходящая группа фтора)
- Информация о материале
- Germán Fernández
- РЕАКЦИИ ЗАМЕЩЕНИЯ (SN1)
- Просмотров: 38519
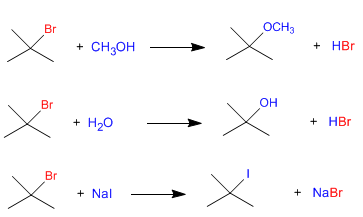
Поскольку медленной стадией мономолекулярного нуклеофильного замещения (S N 1) является диссоциация субстрата, а на второй стадии действует нуклеофил, скорость реакции не зависит от нуклеофила. Следующие три реакции протекают с одинаковой скоростью, поскольку они начинаются с одного и того же субстрата.
Очевидно, необходимо, чтобы другие факторы, такие как растворитель, были одинаковыми в трех реакциях.
- Информация о материале
- Germán Fernández
- РЕАКЦИИ ЗАМЕЩЕНИЯ (SN1)
- Просмотров: 76249
- Информация о материале
- Germán Fernández
- РЕАКЦИИ ЗАМЕЩЕНИЯ (SN1)
- Просмотров: 49771