TEORI STEREOKIMIA
- Detail
- Germán Fernández
- TEORI STEREOKIMIA
- Dilihat: 2032
definisi isomer
Molekul yang memiliki rumus molekul sama tetapi berbeda strukturnya disebut isomer. Ini diklasifikasikan sebagai isomer struktural dan stereoisomer.
isomer struktural
Isomer struktural berbeda dalam cara atom bergabung dan pada gilirannya diklasifikasikan menjadi isomer rantai posisi dan fungsional.
stereoisomer
Stereoisomer memiliki semua ikatan identik dan dibedakan oleh susunan spasial kelompok. Mereka diklasifikasikan sebagai isomer cis-trans atau geometris, enantiomer dan diastereoisomer.
pusat kiral atau asimetris
Sebuah atom yang terikat pada empat substituen berbeda disebut pusat kiral atau asimetris. Molekul yang memiliki pusat kiral memiliki bayangan cermin yang tidak dapat ditumpangkan, yang disebut enansiomer.
aktivitas optik
Enansiomer memiliki hampir semua sifat fisik yang identik, kecuali aktivitas optik. Salah satu enansiomer memutar cahaya terpolarisasi ke kanan (tangan kanan) dan yang lainnya memutar cahaya terpolarisasi ke kiri (tangan kiri).
stereokimia dalam reaksi
Reaksi halogenasi radikal pada molekul di mana pusat kiral dapat dibentuk menghasilkan campuran enantiomer dalam jumlah yang sama atau diastereoisomer dalam proporsi yang berbeda.
pemisahan enansiomer
Enansiomer memiliki hampir semua sifat fisik yang sama, berbeda dalam cahaya terpolarisasi rotasi, tetapi memiliki titik leleh dan titik didih yang sama serta kelarutan yang identik. Oleh karena itu, kami tidak dapat menerapkan metode pemisahan tradisional dan kami harus menggunakan teknik khusus. Pemisahan melalui diastereoisomer, terdiri dari mengubah campuran enansiomer menjadi campuran diastereoisomer dengan menambahkan reagen kiral, diastereoisomer mudah dipisahkan dengan metode fisik.
- Detail
- Germán Fernández
- TEORI STEREOKIMIA
- Dilihat: 111275
Stereokimia adalah studi tentang senyawa organik di ruang angkasa. Untuk memahami sifat-sifat senyawa organik, perlu mempertimbangkan ketiga dimensi spasial. 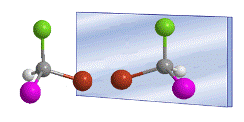 Basis stereokimia diletakkan oleh Jacobus van't Hoff dan Le Bel, pada tahun 1874. Mereka secara terpisah mengusulkan bahwa empat substituen karbon diarahkan ke simpul tetrahedron, dengan karbon di tengah tetrahedron. .
Basis stereokimia diletakkan oleh Jacobus van't Hoff dan Le Bel, pada tahun 1874. Mereka secara terpisah mengusulkan bahwa empat substituen karbon diarahkan ke simpul tetrahedron, dengan karbon di tengah tetrahedron. .
- Detail
- Germán Fernández
- TEORI STEREOKIMIA
- Dilihat: 293688
Isomer adalah molekul yang memiliki rumus molekul yang sama tetapi struktur yang berbeda. Ini diklasifikasikan sebagai isomer struktural dan stereoisomer. Isomer struktural berbeda dalam cara atom mereka terikat dan diklasifikasikan ke dalam rantai, posisi, dan isomer fungsi. Sebagai contoh, mari gambarkan isomer struktur dari rumus C 2 H 6 O .

[1] Etanol
[2] Dimetil eter
- Detail
- Germán Fernández
- TEORI STEREOKIMIA
- Dilihat: 265715
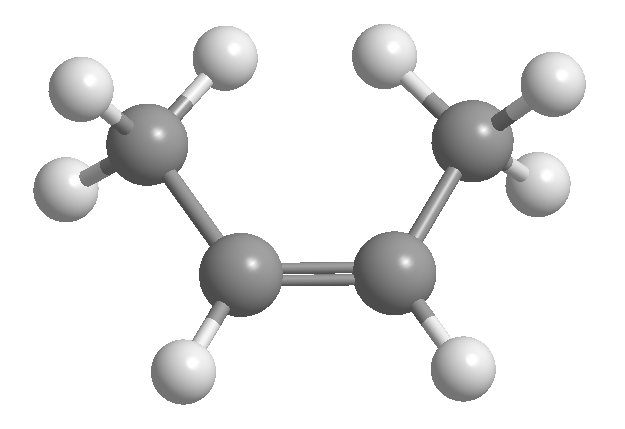
Isomerisme Cis-trans atau geometris disebabkan oleh rotasi terbatas di sekitar ikatan karbon-karbon. Pembatasan ini mungkin karena adanya ikatan rangkap atau siklus. Jadi, 2-butena dapat berada dalam bentuk dua isomer, yang disebut cis dan trans. Isomer dengan hidrogen pada sisi yang sama disebut cis, dan isomer dengan sisi yang berlawanan disebut trans.

[1] cis -2-butena
[2] trans -2-butena
- Detail
- Germán Fernández
- TEORI STEREOKIMIA
- Dilihat: 159996
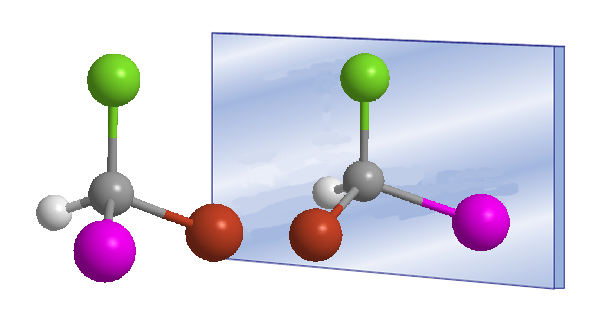
Kata kiral diperkenalkan oleh William Thomson (Lord Kelvin) pada tahun 1894 untuk menunjuk objek yang tidak dapat ditumpangkan dengan bayangan cerminnya. Diterapkan pada kimia organik, kita dapat mengatakan bahwa sebuah molekul adalah kiral ketika ia dan bayangan cerminnya tidak dapat ditumpangkan.
- Detail
- Germán Fernández
- TEORI STEREOKIMIA
- Dilihat: 107438
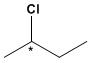 Senyawa dengan karbon asimetris, seperti 2-klorobutana, dapat berbentuk dua isomer.
Senyawa dengan karbon asimetris, seperti 2-klorobutana, dapat berbentuk dua isomer.
- Detail
- Germán Fernández
- TEORI STEREOKIMIA
- Dilihat: 4970
Jumlah maksimum stereoisomer yang dimiliki suatu molekul dapat dihitung dengan rumus (2 n ), di mana n menyatakan jumlah karbon asimetris. Jadi, sebuah molekul dengan 2 pusat kiral memiliki 4 stereoisomer.
Contoh 1. Gambarkan kemungkinan stereoisomer dari 2-Bromo-3-klorobutana.
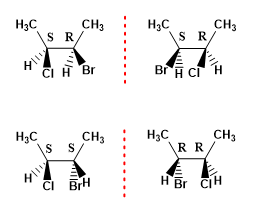
- Detail
- Germán Fernández
- TEORI STEREOKIMIA
- Dilihat: 128966
Nomenklatur diperlukan untuk membedakan stereoisomer molekul. Jadi, dalam kasus 2-Klorobutana, notasi harus membedakan satu enansiomer dari yang lain. Cahn, Ingold, dan Prelog mengembangkan beberapa aturan yang memungkinkan kita membedakan beberapa stereoisomer dari yang lain, yang saya jelaskan di bawah.
- Detail
- Germán Fernández
- TEORI STEREOKIMIA
- Dilihat: 97953
Molekul yang memiliki bidang simetri atau pusat inversi dapat ditumpangkan dengan bayangan cerminnya. Mereka dikatakan sebagai molekul akiral.
- Detail
- Germán Fernández
- TEORI STEREOKIMIA
- Dilihat: 136024
Aktivitas optik adalah kemampuan zat kiral untuk memutar bidang cahaya terpolarisasi. Itu diukur menggunakan alat yang disebut polarimeter.
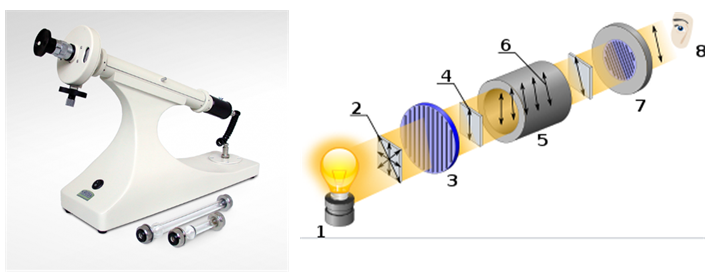
[1 ] Sumber cahaya
[2 ] Cahaya tak terpolarisasi
[3 ] Pempolarisasi linier
[4 ] Cahaya terpolarisasi linier
[5 ] Kuvet sampel
[6 ] Rotasi dalam cahaya terpolarisasi
[7 ] Penganalisis
- Detail
- Germán Fernández
- TEORI STEREOKIMIA
- Dilihat: 136972
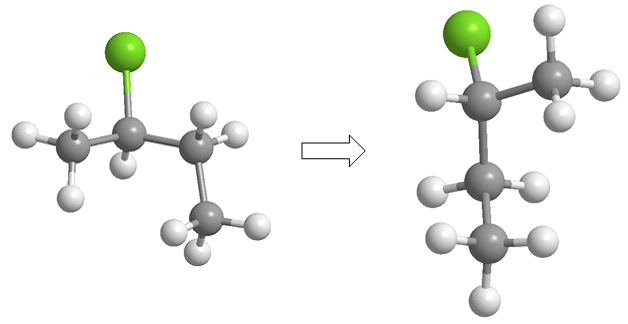
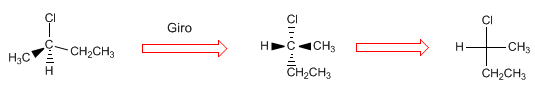
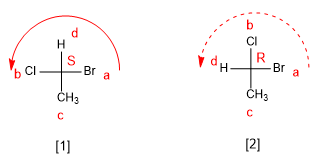
Memproyeksikan terdiri dari menggambar molekul dalam dua dimensi (bidang). Dalam proyeksi Fischer, molekul digambar dalam bentuk salib dengan substituen yang mengarah ke dasar bidang secara vertikal dan kelompok yang keluar ke arah kita secara horizontal, titik perpotongan kedua garis mewakili karbon yang diproyeksikan.
- Detail
- Germán Fernández
- TEORI STEREOKIMIA
- Dilihat: 93342
- Detail
- Germán Fernández
- TEORI STEREOKIMIA
- Dilihat: 90751
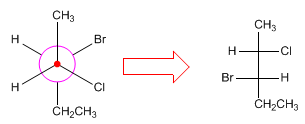
Untuk mengubah proyeksi Newman menjadi proyeksi Fischer, bentuk spasial molekul digambar, menyusunnya dalam konformasi gerhana untuk membuat proyeksi Fischer.
- Detail
- Germán Fernández
- TEORI STEREOKIMIA
- Dilihat: 89657
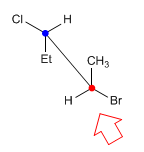 Pada proyeksi kuda-kuda (disebut juga perspektif) garis pengamatan membentuk sudut 45º dengan ikatan karbon-karbon. Karbon yang paling dekat dengan pengamat ada di bawah dan di kanan. Sedangkan yang terjauh ada di kiri atas.
Pada proyeksi kuda-kuda (disebut juga perspektif) garis pengamatan membentuk sudut 45º dengan ikatan karbon-karbon. Karbon yang paling dekat dengan pengamat ada di bawah dan di kanan. Sedangkan yang terjauh ada di kiri atas.
- Detail
- Germán Fernández
- TEORI STEREOKIMIA
- Dilihat: 3799
Kita akan melihat bagaimana reaksi kimia dapat memperkenalkan kiralitas dalam molekul, memperoleh produk dalam bentuk campuran rasemat atau campuran diastereoisomer.
Butana halogenat dengan adanya bromin dan cahaya, pada karbon 2, membentuk campuran enansiomer. Bentuk radikal menghadirkan wajah enansiotopik, yang terhalogenasi dengan probabilitas yang sama, sehingga menimbulkan campuran rasemat (enansiomer dalam proporsi yang sama).
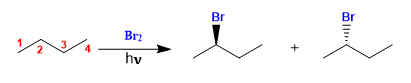
Mekanisme reaksi ini terdiri dari tiga tahap: inisiasi, propagasi, dan terminasi. Perbanyakan adalah langkah yang menentukan stereokimia produk akhir.
halogenasi butana
Tahap 1. Inisiasi
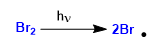
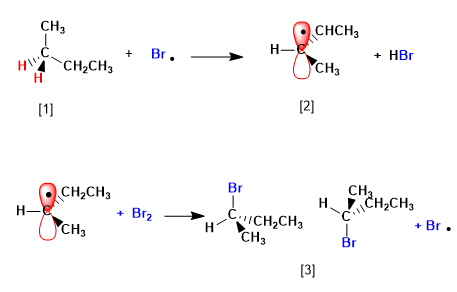
Tahap 2. Perbanyakan
- Detail
- Germán Fernández
- TEORI STEREOKIMIA
- Dilihat: 3969
reaksi stereoselektif
- Detail
- Germán Fernández
- TEORI STEREOKIMIA
- Dilihat: 3279
Kesulitan dalam memisahkan ras