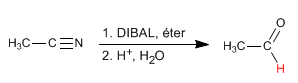NITRIL-THEORIE
- Details
- Germán Fernández
- NITRIL-THEORIE
- Zugriffe: 41888
Die IUPAC benennt Nitrile, indem sie das Suffix -Nitril an den Namen des Alkans mit der gleichen Anzahl an Kohlenstoffatomen anhängt.
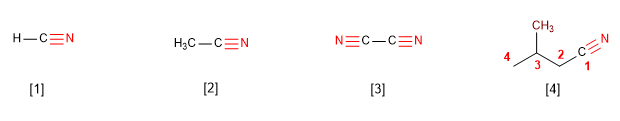
[1] Methannitril
[2] Ethanonitril
[3] Ethandinitril
[4] 3-Methylbutannitril
- Details
- Germán Fernández
- NITRIL-THEORIE
- Zugriffe: 47267
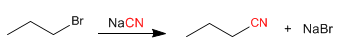
a) Aus Halogenalkanen: Nitrile können aus Halogenalkanen durch SN2-Verfahren hergestellt werden. Die Reaktion zeigt eine gute Leistung mit primären und sekundären Substraten, die tertiären werden bevorzugt eliminiert, wobei Alkene gebildet werden.
- Details
- Germán Fernández
- NITRIL-THEORIE
- Zugriffe: 53121
Nitrile hydrolysieren in sauren Medien unter Erhitzen und werden zu Carbonsäuren und Ammoniumsalzen. Die Hydrolyse von Nitrilen ist ein irreversibler Prozess.
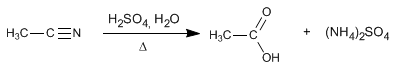
- Details
- Germán Fernández
- NITRIL-THEORIE
- Zugriffe: 39902
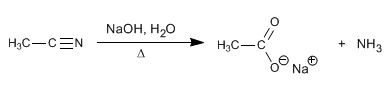
Die Nitrile werden mit wässriger Soda unter Erhitzen hydrolysiert, um Carboxylate und Ammoniak zu bilden.
- Details
- Germán Fernández
- NITRIL-THEORIE
- Zugriffe: 26305
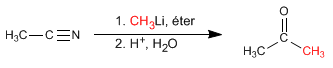
- Details
- Germán Fernández
- NITRIL-THEORIE
- Zugriffe: 16789
Nitrile präsentieren Wasserstoffatome für Säuren, die mit starken Basen entfernt werden können, wobei Nitrilenolate gebildet werden. Diese Wasserstoffe haben einen pKa von 25.
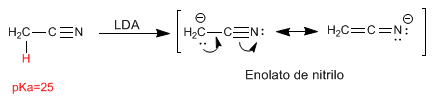
- Details
- Germán Fernández
- NITRIL-THEORIE
- Zugriffe: 31588
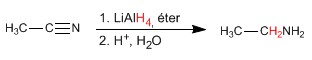
- Details
- Germán Fernández
- NITRIL-THEORIE
- Zugriffe: 23978
DIBAL (Diisobutylaluminiumhydrid) reduziert Nitrile zu Aldehyden