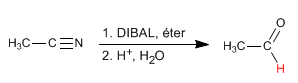THÉORIE DES NITRILES
- Détails
- Germán Fernández
- THÉORIE DES NITRILES
- Affichages : 43800
L'IUPAC nomme les nitriles en ajoutant le suffixe -nitrile au nom de l'alcane avec le même nombre de carbones.
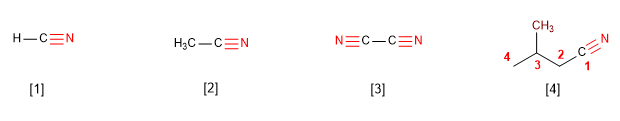
[1] Méthanénitrile
[2] Éthanonitrile
[3] Éthanedinitrile
[4] 3-Méthylbutanenitrile
- Détails
- Germán Fernández
- THÉORIE DES NITRILES
- Affichages : 47475
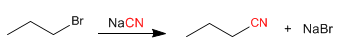
a) A partir d'haloalcanes : Les nitriles peuvent être préparés à partir d'haloalcanes, par les procédés SN2. La réaction donne de bons résultats avec les substrats primaires et secondaires, les tertiaires sont préférentiellement éliminés, formant des alcènes.
- Détails
- Germán Fernández
- THÉORIE DES NITRILES
- Affichages : 46799
Les nitriles s'hydrolysent en milieu acide, sous chauffage, devenant des acides carboxyliques et des sels d'ammonium. L'hydrolyse des nitriles est un processus irréversible.
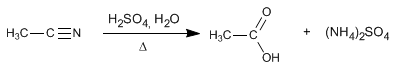
- Détails
- Germán Fernández
- THÉORIE DES NITRILES
- Affichages : 37404
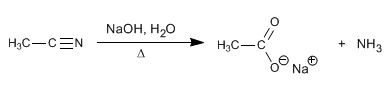
Les nitriles sont hydrolysés avec de la soude aqueuse, sous chauffage, pour former des carboxylates et de l'ammoniac.
- Détails
- Germán Fernández
- THÉORIE DES NITRILES
- Affichages : 25913
Les nitriles réagissent avec le lithium ou le magnésium organométallique, pour former des cétones, après une étape d'hydrolyse acide.
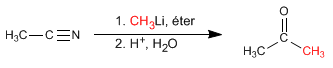
Lire la suite : Réaction des nitriles avec les organométalliques
- Détails
- Germán Fernández
- THÉORIE DES NITRILES
- Affichages : 16802
Les nitriles présentent des hydrogènes aux acides qui peuvent être éliminés avec des bases fortes, formant des énolates de nitrile. Ces hydrogènes ont un pKa de 25.
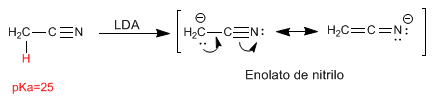
- Détails
- Germán Fernández
- THÉORIE DES NITRILES
- Affichages : 29176
L'hydrure de lithium et d'aluminium réduit les nitriles en amines. La réaction est effectuée en milieu éthéré, suivie d'une hydrolyse acide. 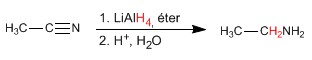
- Détails
- Germán Fernández
- THÉORIE DES NITRILES
- Affichages : 23112
Le DIBAL (hydrure de diisobutylaluminium) réduit les nitriles en aldéhydes