Sistemas alílicos podem atuar como substratos em reações de substituição nucleofílica. Assim, a reação do 3-cloro-1-buteno com água produz dois álcoois alílicos.
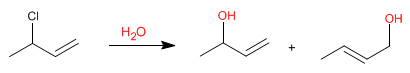
Como a água é um nucleófilo ruim, o mecanismo de substituição será unimolecular (S N 1), com a particularidade de encontrar o grupo abandonante (cloro) em posição alílica.
Descrevemos o mecanismo abaixo:
Fase 1 . Formação do carbocátion alílico pela perda do grupo abandonador. O carbocátion é estabilizado por ressonância, sendo o híbrido formado por duas estruturas ressonantes.
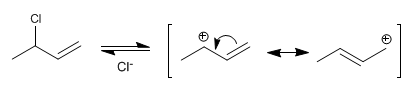
Fase 2 . Ataque nucleofílico de água no carbocátion formado. O carbocátion existe em duas estruturas, que ao serem atacadas formam dois produtos distintos. A estrutura mais importante é aquela que localiza a carga no carbono secundário, obtendo dele o produto majoritário (condições de baixa temperatura e tempos de reação curtos).
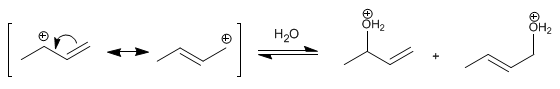
Fase 3 . desprotonação A água perde um próton tornando-se álcool.
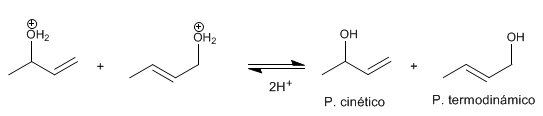
O produto mais estável (ligação dupla mais substituída) é chamado termodinâmico . O produto menos estável é chamado cinético .