Les systèmes allyliques peuvent agir comme substrats dans les réactions de substitution nucléophile. Ainsi, la réaction du 3-chloro-1-butène avec de l'eau produit deux alcools allyliques.
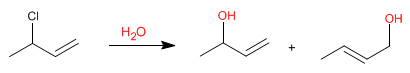
L'eau étant un mauvais nucléophile, le mécanisme de substitution sera unimoléculaire (S N 1), avec la particularité de retrouver le groupe partant (chloro) sur une position allylique.
Nous décrivons le mécanisme ci-dessous :
Étape 1 . Formation du carbocation allylique par perte du groupe partant. Le carbocation est stabilisé par résonance, l'hybride étant formé de deux structures résonnantes.
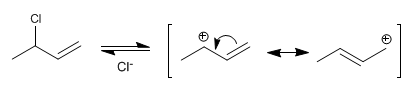
Étape 2 . Attaque nucléophile de l'eau sur le carbocation formé. Le carbocation existe dans deux structures qui, lorsqu'elles sont attaquées, forment deux produits différents. La structure la plus importante est celle qui localise la charge sur le carbone secondaire, en obtenant le produit majoritaire (conditions de basse température et temps de réaction courts).
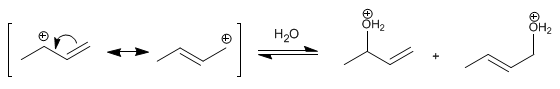
Étape 3 . déprotonation L'eau perd un proton en devenant alcool.
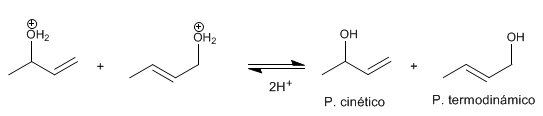
Le produit le plus stable (double liaison la plus substituée) est dit thermodynamique . Le produit le moins stable est appelé cinétique .