Sistem alilik dapat bertindak sebagai substrat dalam reaksi substitusi nukleofilik. Jadi, reaksi 3-kloro-1-butena dengan air menghasilkan dua alkohol alilik.
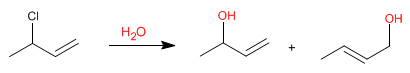
Karena air adalah nukleofil yang buruk, mekanisme substitusi akan bersifat unimolekuler ( SN 1), dengan kekhasan menemukan gugus pergi (kloro) pada posisi alilik.
Kami menjelaskan mekanismenya di bawah ini:
Tahap 1 . Pembentukan karbokation alilik dengan hilangnya gugus pergi. Karbokation distabilkan oleh resonansi, hibrida dibentuk oleh dua struktur resonansi.
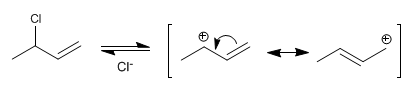
Tahap 2 . Serangan nukleofilik air pada karbokation yang terbentuk. Karbokation ada dalam dua struktur, yang ketika diserang membentuk dua produk yang berbeda. Struktur terpenting adalah yang menempatkan muatan pada karbon sekunder, memperoleh produk mayoritas darinya (kondisi suhu rendah dan waktu reaksi singkat).
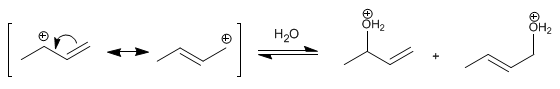
Tahap 3 . deprotonasi Air kehilangan proton menjadi alkohol.
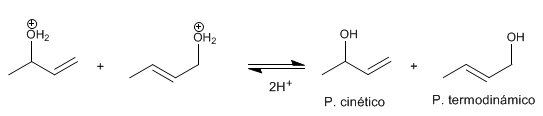
Produk paling stabil (ikatan rangkap paling tersubstitusi) disebut termodinamika . Produk yang paling tidak stabil disebut kinetik .