1. Ethers d'alcools primaires
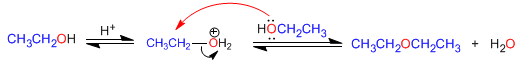
Les éthers symétriques peuvent être préparés par condensation d'alcools. La réaction est effectuée sous chauffage (140°C) et avec une catalyse acide. Ainsi, deux molécules d'éthanol se condensent pour former de l'éther diéthylique.
Le mécanisme de réaction se produit dans les étapes suivantes :
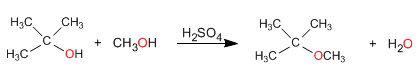
2. L'un des alcools est secondaire ou tertiaire
Dans ce cas, la réaction se déroule dans des conditions plus douces, par des mécanismes S N 1 .
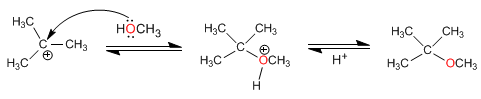
Le mécanisme se produit avec la formation d'un carbocation tertiaire très stable
Étape 1. Protonation de l'alcool tertiaire
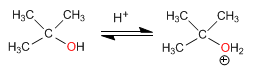
Étape 2. Formation du carbocation par perte d'eau
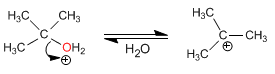
Étape 3. Attaque nucléophile du méthanol