THÉORIE DE L'ALCYNE
- Détails
- Germán Fernández
- THÉORIE DE L'ALCYNE
- Affichages : 93907
Les alcynes sont des hydrocarbures qui contiennent des triples liaisons carbone-carbone. La formule moléculaire générale des alcynes acycliques est C n H 2n-2 et son degré d'insaturation est de deux. L'acétylène ou éthyne est l'alcyne le plus simple, il a été découvert par Berthelot en 1862.
- Détails
- Germán Fernández
- THÉORIE DE L'ALCYNE
- Affichages : 112782
Règle 1. Les alcynes répondent à la formule $C_nH_{2n-2}$ et sont nommés en remplaçant le suffixe -ane de l'alcane ayant le même nombre de carbones par -yne.
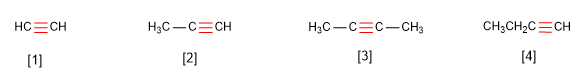
- Détails
- Germán Fernández
- THÉORIE DE L'ALCYNE
- Affichages : 147899
Les alcynes ont des propriétés physiques similaires aux alcanes et aux alcènes. Ils sont peu solubles dans l'eau, ont une faible densité et ont des points d'ébullition bas. Cependant, les alcynes sont plus polaires en raison de la plus grande attraction qu'un carbone sp exerce sur les électrons, par rapport à un carbone sp 3 ou sp 2 .
- Détails
- Germán Fernández
- THÉORIE DE L'ALCYNE
- Affichages : 82046
La liaison carbone-hydrogène des alcynes terminaux est polarisée et présente une légère tendance à s'ioniser.
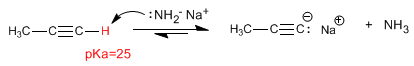
- Détails
- Germán Fernández
- THÉORIE DE L'ALCYNE
- Affichages : 84631
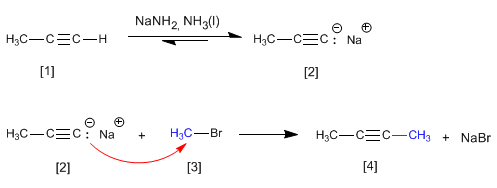
Comme nous l'avons vu au point précédent, les alcynes terminaux ont des hydrogènes acides qui peuvent être éliminés par des bases fortes, formant des acétylures (base conjuguée de l'alcyne). Les acétylures sont de bons nucléophiles et donnent des mécanismes de substitution nucléophile avec des substrats primaires.
- Détails
- Germán Fernández
- THÉORIE DE L'ALCYNE
- Affichages : 62416
Les alcynes peuvent être préparés par double déshydrohalogénation de dihaloalcanes vicinaux ou géminés.
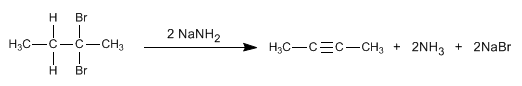
Lire la suite : Préparation des alcynes par double élimination
- Détails
- Germán Fernández
- THÉORIE DE L'ALCYNE
- Affichages : 93327
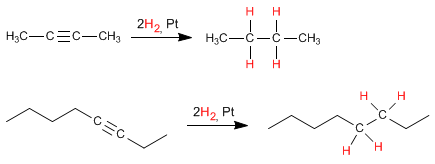
Les alcynes sont hydrogénés avec deux équivalents d'hydrogène, en présence d'un catalyseur métallique finement divisé, pour former des alcanes. Les catalyseurs les plus couramment utilisés sont : le platine, le palladium, le rhodium...
- Détails
- Germán Fernández
- THÉORIE DE L'ALCYNE
- Affichages : 66783
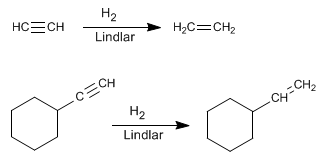
Lire la suite : Hydrogénation des alcynes avec le catalyseur Lindlar
- Détails
- Germán Fernández
- THÉORIE DE L'ALCYNE
- Affichages : 55898
Une alternative à l'hydrogénation avec le catalyseur de Lindlar est la réduction des alcynes avec du sodium ou du lithium dans l'ammoniac liquide, la différence réside dans l'alcène obtenu. Ainsi, l'hydrogénation avec le catalyseur de Lindlar produit des alcènes cis, tandis que l'hydrogénation avec du sodium dans l'ammoniac liquide génère des alcènes trans.
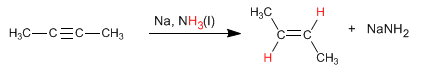
Lire la suite : Hydrogénation des alcynes avec du sodium dans l'ammoniac liquide
- Détails
- Germán Fernández
- THÉORIE DE L'ALCYNE
- Affichages : 93789
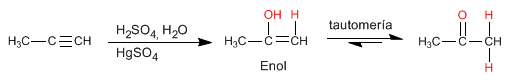
Les alcynes réagissent avec l'acide sulfurique aqueux en présence d'un catalyseur au mercure pour former des énols. L'énol s'isomérise (tautomérise) rapidement dans les conditions de réaction pour donner des aldéhydes ou des cétones.
- Détails
- Germán Fernández
- THÉORIE DE L'ALCYNE
- Affichages : 56042
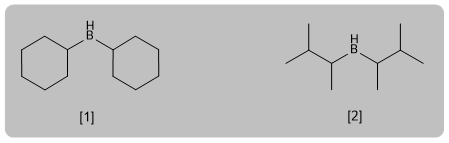
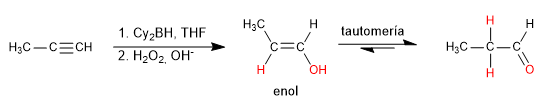
L'hydroboration est l'hydratation anti-Markovnikov d'un alcyne. Un borane encombré (dicyclohexylborane ou diisoamylborane) est utilisé comme réactif, obtenant un énol qui se tautomérise en aldéhyde ou en cétone. Les alcynes terminaux donnent naissance aux aldéhydes, les internes aux cétones.
- Détails
- Germán Fernández
- THÉORIE DE L'ALCYNE
- Affichages : 78628
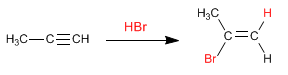
Semblables aux alcènes, les alcynes ajoutent des halogénures d'hydrogène (HBr, HCl, HI) à la triple liaison pour former des halogénures d'alcényle.
- Détails
- Germán Fernández
- THÉORIE DE L'ALCYNE
- Affichages : 95272
Les alcynes réagissent avec le chlore et le brome pour former des tétrahaloalcanes. La triple liaison ajoute deux molécules d'halogène, bien qu'il soit possible d'arrêter la réaction dans l'alcène en ajoutant un seul équivalent halogène. 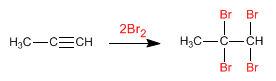
- Détails
- Germán Fernández
- THÉORIE DE L'ALCYNE
- Affichages : 69637
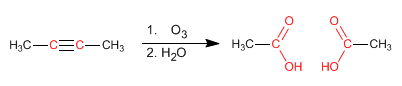
Les alcynes réagissent avec l'ozone pour former des acides carboxyliques. Dans cette réaction, la triple liaison est rompue, transformant chaque carbone de l'alcyne en groupe carboxylique.