THÉORIE DES SYSTÈMES ALLYLIQUES
- Détails
- Germán Fernández
- THÉORIE DES SYSTÈMES ALLYLIQUES
- Affichages : 22977
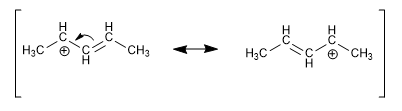
Les charges positives, négatives ou radicalaires en positions proches des doubles liaisons sont délocalisées par résonance, étant particulièrement stables.
- Détails
- Germán Fernández
- THÉORIE DES SYSTÈMES ALLYLIQUES
- Affichages : 42674
Le groupe CH 2 =CHCH 2 - est appelé allyle. Certains composés qui dérivent du groupe allyle sont :
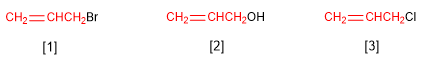
- Détails
- Germán Fernández
- THÉORIE DES SYSTÈMES ALLYLIQUES
- Affichages : 25408
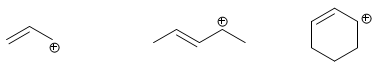
Les carbocations formés sur des carbones situés dans des positions allyliques sont appelés cations allyliques.
- Détails
- Germán Fernández
- THÉORIE DES SYSTÈMES ALLYLIQUES
- Affichages : 16376
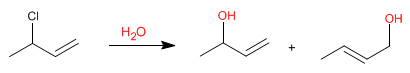
Les systèmes allyliques peuvent agir comme substrats dans les réactions de substitution nucléophile. Ainsi, la réaction du 3-chloro-1-butène avec de l'eau produit deux alcools allyliques.
- Détails
- Germán Fernández
- THÉORIE DES SYSTÈMES ALLYLIQUES
- Affichages : 2764
La formation du carbocation allylique, stabilisé par résonance, permet à la réaction d'évoluer de deux manières qui conduisent aux produits cinétiques et thermodynamiques.
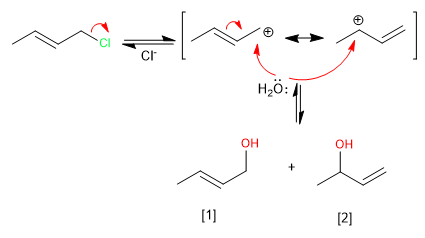
Lire la suite : Contrôle cinétique et thermodynamique dans les systèmes allyliques
- Détails
- Germán Fernández
- THÉORIE DES SYSTÈMES ALLYLIQUES
- Affichages : 2155
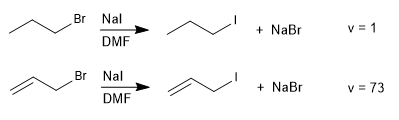
Les réactions S N 2 avec des groupes partants en positions allyliques se déroulent plus rapidement que celles des haloalcanes saturés correspondants.
- Détails
- Germán Fernández
- THÉORIE DES SYSTÈMES ALLYLIQUES
- Affichages : 3123
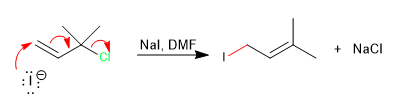
Avec les substrats allyliques tertiaires et dans les conditions de S N 2 (bon solvant nucléophile et aprotique), une réaction concertée se produit par le nucléophile attaquant le carbone de la double liaison avec perte du groupe partant.
- Détails
- Germán Fernández
- THÉORIE DES SYSTÈMES ALLYLIQUES
- Affichages : 1930
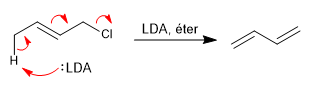
Les bases fortes et encombrées donnent majoritairement E2 avec des systèmes allyliques, déprotonant le carbone situé en position 4 par rapport au groupe partant.
- Détails
- Germán Fernández
- THÉORIE DES SYSTÈMES ALLYLIQUES
- Affichages : 2894
Les halogènes peuvent s'ajouter aux alcènes donnant des dihaloalcanes vicinaux, mais lorsque cette réaction est effectuée à de faibles concentrations d'halogène, les mécanismes radicalaires sont favorisés. Un réactif largement utilisé dans les bromations allyliques est le NBS (N-bromosuccinimide).
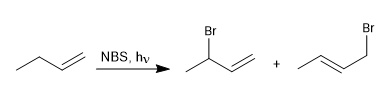
Lire la suite : Réactions radicales dans les systèmes allyliques
- Détails
- Germán Fernández
- THÉORIE DES SYSTÈMES ALLYLIQUES
- Affichages : 2310
Les diènes conjugués ajoutent les acides des halogènes formant des produits cinétiques et thermodynamiques, dont le rapport peut être contrôlé avec les conditions de réaction (température et durée).
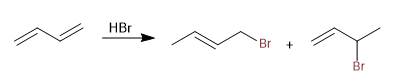
Lire la suite : Addition acide d'halogènes (HX) aux diènes conjugués
- Détails
- Germán Fernández
- THÉORIE DES SYSTÈMES ALLYLIQUES
- Affichages : 2497
Contrairement à l'addition de brome aux alcènes, les diènes conjugués ne forment pas d'ions halonium en raison de la grande stabilité du carbocation formé.
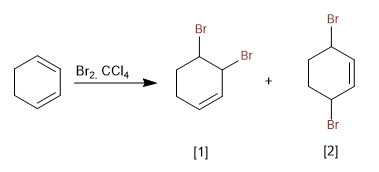
[1 ] Produit d'addition 1,2
[2 ] Produit d'addition 1.4