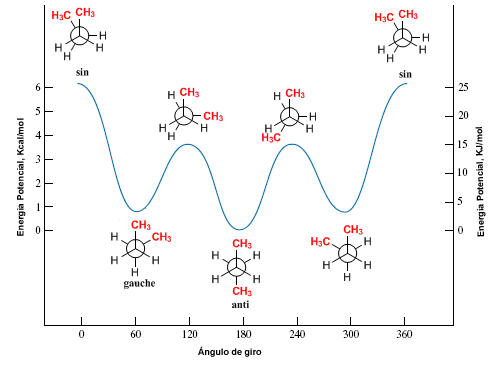
Considérons la liaison C2-C3 du butane. Les virages à 60º autour de ce lien vont générer les éventuelles conformations du butane. Il existe trois conformations d'une importance particulière appelées; butane syn , butane anti et butane gauche que nous représentons dans les modèles suivants.
La conformation « anti » du butane est celle dont l'énergie est la plus faible. Les méthyles sont sur les côtés opposés, minimisant les répulsions. 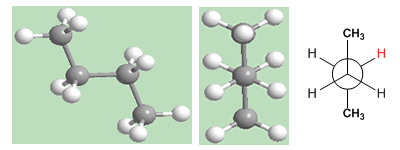
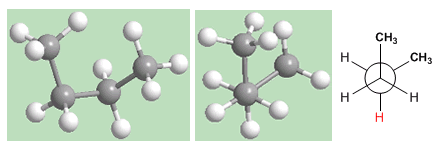
Dans la conformation gauche, la proximité des méthyles donne lieu à une interaction répulsive, appelée interaction gauche. Cette répulsion entre les méthyles est d'environ 3,2 Kcal/mol.
La conformation "syn" est celle qui a la plus haute énergie. Les méthyles se font face et les répulsions (interactions d'éclipse) font que cette conformation a une énergie supérieure de 25 KJ/mol à l'anti conformation. 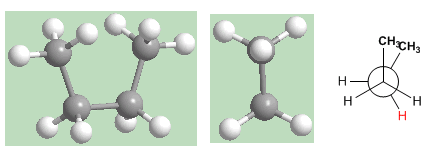
Nous dessinons les conformations butane qui résultent des virages à 60º.
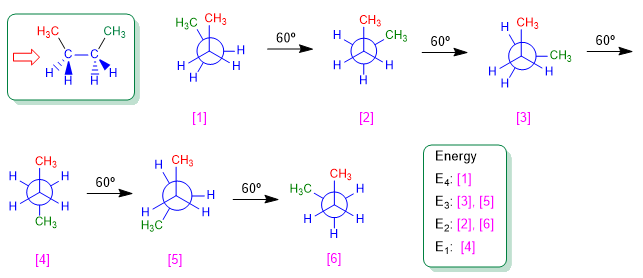
Le diagramme de l'énergie potentielle en fonction de l'angle de rotation pour le butane nous laisse :