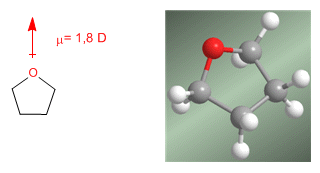
Les éthers sont des molécules de structure similaire à l'eau et aux alcools. L'angle entre les liaisons C- O -C est plus grand que dans l'eau en raison des répulsions stériques entre les groupes volumineux.
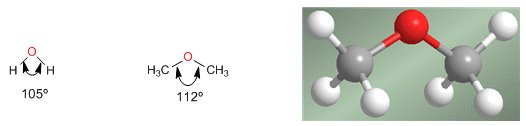
Dans le cas des époxydes, la caractéristique la plus pertinente est la tension de l'anneau due à des angles de liaison très éloignés de 109º, la liaison C- O -C présente un angle de 61º.
Les éthers sont des molécules très polaires. Ainsi, l'éther diéthylique présente un moment dipolaire de 1,2 D. Ce moment dipolaire est encore plus important dans les éthers cycliques (oxacyclopropane, tétrahydrofuranne) qui présentent des moments dipolaires supérieurs à 1,8 D, similaires à l'eau.