THÉORIE DE L'ÉTHER
- Détails
- Germán Fernández
- THÉORIE DE L'ÉTHER
- Affichages : 101650
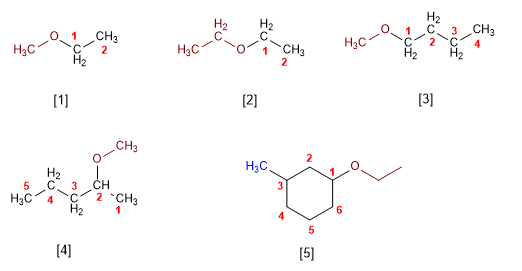
Règle 1. Les éthers peuvent être nommés comme des dérivés alcoxy d'alcanes (nomenclature IUPAC substitutive). La chaîne la plus longue est considérée comme la chaîne principale et l'alcoolate est nommé comme substituant.
- Détails
- Germán Fernández
- THÉORIE DE L'ÉTHER
- Affichages : 72604
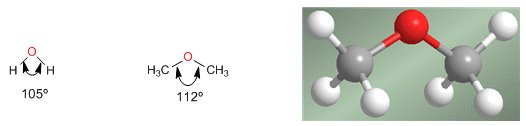
Les éthers sont des molécules de structure similaire à l'eau et aux alcools. L'angle entre les liaisons C- O -C est plus grand que dans l'eau en raison des répulsions stériques entre les groupes volumineux.
Lire la suite : Structure et liaison dans les éthers et les époxydes
- Détails
- Germán Fernández
- THÉORIE DE L'ÉTHER
- Affichages : 176679
Les éthers ont des points d'ébullition inférieurs à ceux des alcools, bien que leur solubilité dans l'eau soit similaire. Compte tenu de leur grande stabilité en milieu basique, ils sont utilisés comme solvants inertes dans de nombreuses réactions.
- Détails
- Germán Fernández
- THÉORIE DE L'ÉTHER
- Affichages : 98750
Lire la suite : Synthèse d'éthers par condensation d'alcools
- Détails
- Germán Fernández
- THÉORIE DE L'ÉTHER
- Affichages : 112249
La réaction entre un haloalcane primaire et un alcoxyde (ou alcool en milieu basique) est la méthode la plus importante pour la préparation des éthers. Cette réaction est connue sous le nom de synthèse de Williamson.
- Détails
- Germán Fernández
- THÉORIE DE L'ÉTHER
- Affichages : 3676
Les éthers peuvent être obtenus en faisant réagir des haloalcanes avec des alcools par le mécanisme S N 1. L'haloalcane doit être secondaire ou tertiaire pour former des carbocations stables.
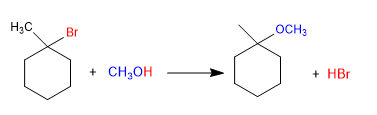
Mécanisme:
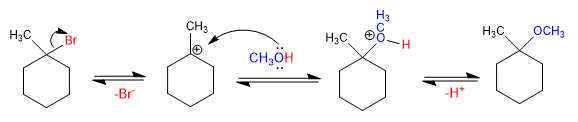
- Détails
- Germán Fernández
- THÉORIE DE L'ÉTHER
- Affichages : 3391
Les alcools peuvent être protégés en les transformant en éthers. Ce procédé est réalisé en faisant réagir l'alcool à protéger avec du tert-butanol en milieu acide sulfurique. La déprotection a lieu en milieu aqueux acide. Voyons un exemple :
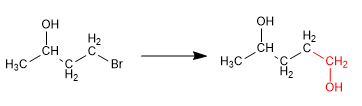
Dans cette synthèse, il est nécessaire de former une liaison carbone-carbone à l'aide de réactifs organométalliques, incompatibles avec l'alcool. Ainsi, l'alcool doit être préalablement protégé pour éviter la décomposition de l'organométallique.
Lire la suite : Les éthers en tant que groupes protecteurs des alcools
- Détails
- Germán Fernández
- THÉORIE DE L'ÉTHER
- Affichages : 8022
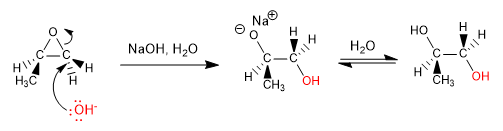
Les époxydes (oxacyclopropanes) sont des éthers cycliques à trois chaînons. Sa principale caractéristique est la tension de l'anneau qui favorise son ouverture aussi bien en milieu basique qu'acide.
Ouverture en milieu basique : Les époxydes s'ouvrent par attaque nucléophile sur le carbone le moins substitué (l'ouverture est régie par des encombrements stériques)