THÉORIE DES ALCÈNES
- Détails
- Germán Fernández
- THÉORIE DES ALCÈNES
- Affichages : 76514
 Les alcènes sont des hydrocarbures qui contiennent des doubles liaisons carbone-carbone. Le mot oléfine est fréquemment utilisé comme synonyme.
Les alcènes sont des hydrocarbures qui contiennent des doubles liaisons carbone-carbone. Le mot oléfine est fréquemment utilisé comme synonyme.
Les alcènes abondent dans la nature. L'éthylène est un composé qui contrôle la croissance des plantes, la germination des graines et la maturation des fruits.
- Détails
- Germán Fernández
- THÉORIE DES ALCÈNES
- Affichages : 185202
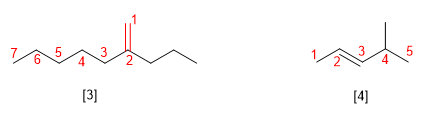
Les alcènes sont nommés en remplaçant la terminaison -ane de l'alcane correspondant par -ène. Les alcènes les plus simples sont l'éthène et le propène, également appelés éthylène et propylène au niveau industriel.

- Détails
- Germán Fernández
- THÉORIE DES ALCÈNES
- Affichages : 124231
 Chaque cycle ou cycle d'une molécule implique la perte de deux hydrogènes par rapport à un alcane de formule C n H 2n+2 . Le degré d'insaturation est le nombre de cycles et de doubles liaisons présents dans une molécule.
Chaque cycle ou cycle d'une molécule implique la perte de deux hydrogènes par rapport à un alcane de formule C n H 2n+2 . Le degré d'insaturation est le nombre de cycles et de doubles liaisons présents dans une molécule.
- Détails
- Germán Fernández
- THÉORIE DES ALCÈNES
- Affichages : 77482
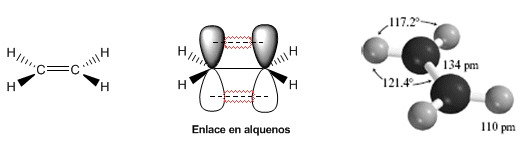
Les modèles suivants montrent la structure, les distances et les angles de liaison de l'éthène. Chacun des carbones de la molécule est $sp^2$ hybridé. Sa géométrie est plate, avec des angles de liaison proches de 120º.
- Détails
- Germán Fernández
- THÉORIE DES ALCÈNES
- Affichages : 130950
Les alcènes ont des points de fusion et d'ébullition proches des alcanes correspondants.
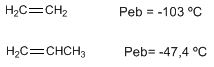
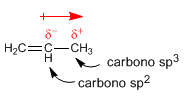
Moment dipolaire dans les alcènes. Dans le carbone $sp^2$, les électrons de l'orbitale s sont plus proches du noyau et sont fortement attirés par lui, de sorte qu'un carbone $sp^2$ a tendance à attirer les électrons vers lui, ce qui génère des moments dipolaires.
- Détails
- Germán Fernández
- THÉORIE DES ALCÈNES
- Affichages : 76065
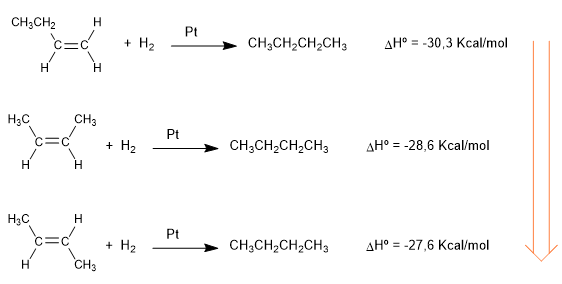
Les chaleurs dégagées dans les réactions d'hydrogénation suivantes nous donnent une idée de la stabilité différente des alcènes.
- Détails
- Germán Fernández
- THÉORIE DES ALCÈNES
- Affichages : 69217
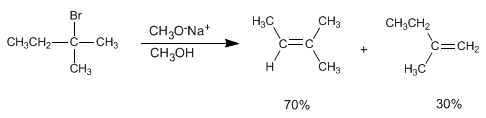
Les alcènes peuvent être préparés à partir d'haloalcanes et d'alkylsulfonates par élimination bimoléculaire (E2). Dans l'exemple suivant, le 2-bromo-2-méthylbutane réagit avec le méthylate de sodium pour former un mélange de 2-méthyl-2-butène et de 2-méthyl-1-butène.
- Détails
- Germán Fernández
- THÉORIE DES ALCÈNES
- Affichages : 128420
Le traitement des alcools avec des acides minéraux à haute température provoque la perte d'eau, qui se produit par les mécanismes E1 ou E2.
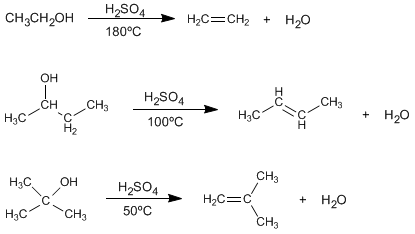
Lire la suite : Synthèse d'alcènes par déshydratation d'alcools