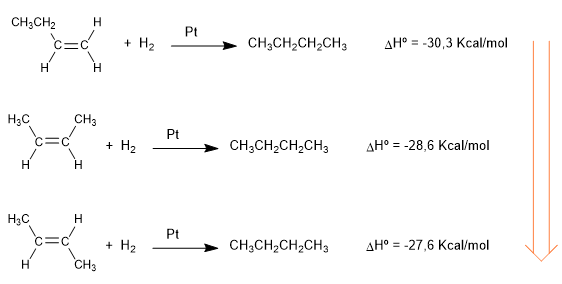
Les chaleurs dégagées dans les réactions d'hydrogénation suivantes nous donnent une idée de la stabilité différente des alcènes.
Stabilité accrue
Les trois alcènes s'hydrogénent pour donner le même alcane (butane). Le 1-butène est l'alcène qui libère le plus d'énergie lors de l'hydrogénation, il est donc le plus instable (il a plus d'énergie). Les cis et trans -2-butène ont une plus grande stabilité car ce sont des alcènes plus substitués. L'interaction entre les chaînes qui entourent l'alcène et la double liaison (hyperconjugaison) le stabilise, abaissant son énergie.
Comme on peut le voir, le cis -2-butène est plus instable que le trans , en raison des répulsions stériques entre les méthyles.
L'ordre de stabilité des alcènes est le suivant :
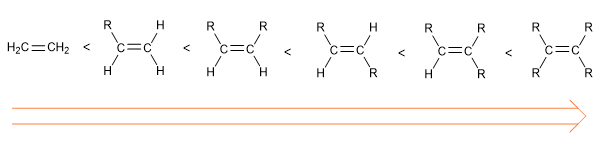
Stabilité accrue