La liaison carbone-hydrogène des alcynes terminaux est polarisée et présente une légère tendance à s'ioniser.
L'hydrogène propyne est faiblement acide, avec un pKa = 25. En utilisant des bases fortes (NaH, LDA, NH 2 - ), il peut être déprotoné, obtenant sa base conjuguée - propynyl sodium - une espèce très basique et nucléophile.
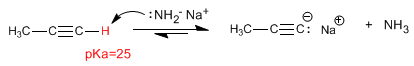
Le propynyl sodium généré dans la réaction ci-dessus peut agir comme un nucléophile attaquant les haloalcanes primaires via le mécanisme SN2.
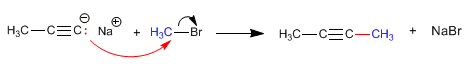
Les bases dérivées des alcools et de l'eau sont trop faibles pour déprotoner les alcynes, et les équilibres acido-basiques sont fortement décalés vers la gauche.
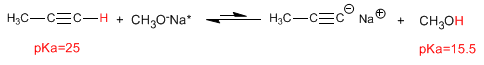
Un équilibre acide-base est déplacé vers l'acide conjugué avec la valeur de pKa la plus élevée.
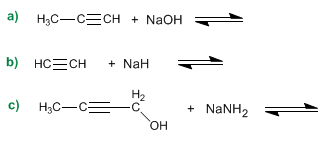
Exemple : compléter les équilibres acido-basiques suivants