Le méthane (CH4), l'éthane (C2H6 ) et le propane (C3H8) sont des alcanes avec une seule structure possible. Cependant, il existe deux alcanes de formule C4H10 ; butane et 2-méthylpropane. Ces alcanes de même formule mais de structures différentes sont appelés isomères.

[1] Butane
[2] 2-Méthylpropane
Le n-butane et l'isobutane ont la même formule mais diffèrent par la façon dont leurs atomes sont liés - ce sont des isomères structuraux -. Leur structure différente leur confère des propriétés différentes, ainsi, ils diffèrent d'environ 20 ºC dans leur point de fusion et d'environ 10 ºC dans leur point d'ébullition.
Il existe trois isomères de formule C5H12 . L'isomère linéaire est appelé n-pentane. Les ramifiés sont l'isopentane (2-méthylbutane) et le néopentane (2,2-diméthylpropane).
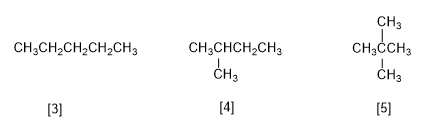
[3] Pentane
[4] 2-Méthylbutane
[5] 2,2-Diméthylpropane
Il existe cinq isomères constitutionnels de formule C6H14 :
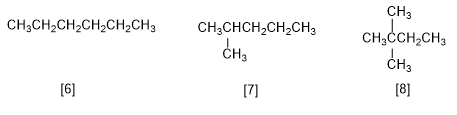
[6 ] Hexane
[7] 2-Méthylpentane
[8] 2,2-Diméthylbutane
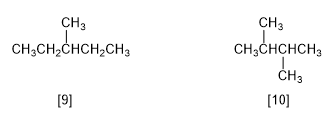
[9] 3-Méthylpentane
[10] 2,3-Diméthylbutane
Lorsque le nombre de carbones augmente, le nombre d'isomères augmente de façon exponentielle. Il existe plus de 360 000 isomères de formule C20H42 et plus de 62 millions de formule C40H82 .