Lorsqu'un ester avec des hydrogènes a est traité avec un équivalent de base (alcoolate), il se condense pour former un produit de la famille des 3-cétoesters. Ce type de réaction est connu sous le nom de condensation de Claisen.
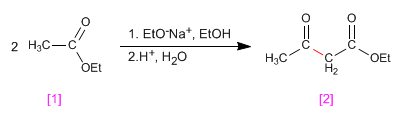
L'éthanoate d'éthyle [1] se condense en présence d'un équivalent d'éthoxyde dans l'éthanol suivi d'une étape acide, pour former l'éthyle [2] 3-oxobutanoate (3-céto ester)
Le mécanisme de la condensation de Claisen se déroule de manière similaire à celui de la condensation aldolique. Dans une première étape, un énolate d'ester se forme qui se condense sur le carbonyle d'une autre molécule d'ester. Les équilibres sont défavorables et il faut une dernière étape acido-basique pour les déplacer.
Étape 1. Formation de l'énolate d'ester
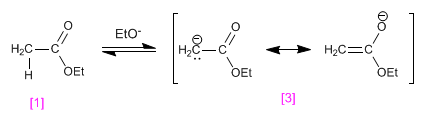
Étape 2. Ajout nucléophile
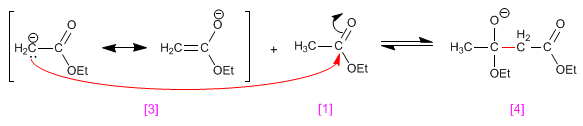
Étape 3. Élimination de l'éthylate
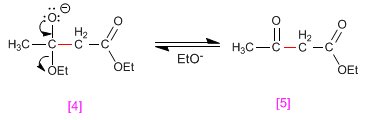
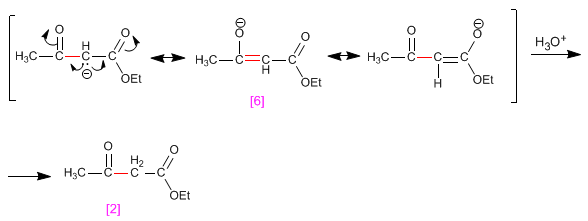
Etape 4. Transformation du 3-cétoester en son énolate. Cette étape est le premier équilibre favorable du Claisen et elle déplace tous les équilibres précédents vers le produit final.
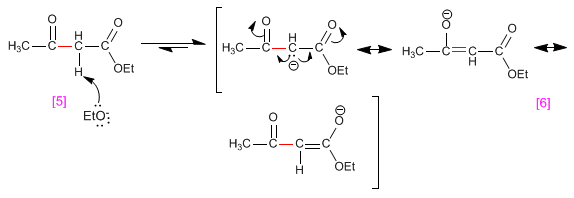
Étape 5. Protonation de l'énolate céto-ester