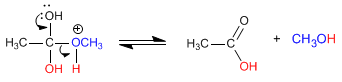Les esters sont hydrolysés en milieu aqueux, sous catalyse acide ou basique, pour donner des acides carboxyliques et des alcools.
En milieu acide, l'hydrolyse des esters peut s'écrire par l'équation chimique suivante :
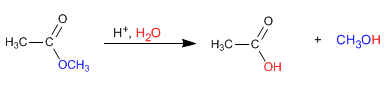
Le mécanisme de l'hydrolyse acide se déroule dans les étapes suivantes :
Étape 1. Protonation de l'ester
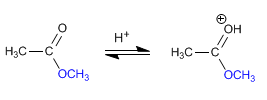
Étape 2. Ajout nucléophile d'eau au carbonyle
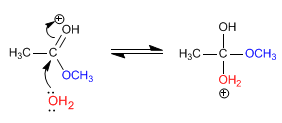
Étape 3. Équilibre acido-basique, qui transforme le méthylate en un bon groupe partant (méthanol).
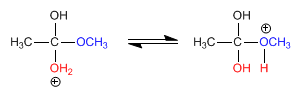
Étape 4. Élimination du méthanol