TEORIA DEI CARBOIDRATI
- Dettagli
- Germán Fernández
- TEORIA DEI CARBOIDRATI
- Visite: 3393
I carboidrati più semplici sono zuccheri o saccaridi, sono aldeidi poliidrossilate o chetoni. Sono classificati come aldosi, se hanno la funzione aldeidica, e chetosi, se hanno la funzione chetonica.
Gli aldosi sono classificati in base al numero di atomi di carbonio in: aldotriosi, aldotetrosi, aldopentosi e aldoesosi.
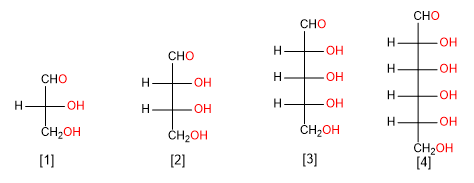
[1] Aldoso di tre atomi di carbonio (aldotrioso)
[2] Aldoso di quattro atomi di carbonio (aldotetroso)
[3] Aldoso di cinque atomi di carbonio (aldopentoso)
[4] Aldoso di sei atomi di carbonio (aldoesoso)
- Dettagli
- Germán Fernández
- TEORIA DEI CARBOIDRATI
- Visite: 36726
La tabella seguente raccoglie i monosaccaridi naturali che contengono un gruppo aldeidico, chiamati aldosi. La tabella è costruita partendo dall'aldosio più piccolo, la gliceraldeide (aldotriosio). L'eritrosio e il treosio (aldotetrosi) si ottengono dalla gliceraldeide mediante l'aggiunta di un quarto carbonio. L'aggiunta di un quinto carbonio agli aldotetrosi dà origine agli aldopentosi, e questi a loro volta formano gli aldoesosi aggiungendo un sesto carbonio.
- Dettagli
- Germán Fernández
- TEORIA DEI CARBOIDRATI
- Visite: 22139
I chetosi naturali sono una famiglia di monosaccaridi che contengono un gruppo chetonico in posizione 2 della catena.
- Dettagli
- Germán Fernández
- TEORIA DEI CARBOIDRATI
- Visite: 42317
Durante lo studio della rotazione ottica della gliceraldeide naturale, è stato osservato che coincideva con l'enantiomero destrogiro ed è stato chiamato D-gliceraldeide. L'enantiomero levogiro, non presente in natura, è stato denominato L-gliceraldeide.
- Dettagli
- Germán Fernández
- TEORIA DEI CARBOIDRATI
- Visite: 36596
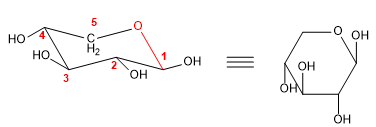
La proiezione di Haworth consente di disegnare le forme emiacetaliche nel piano. Nel caso dei furanosi abbiamo già usato questa notazione negli esempi precedenti, quindi disegnerò un esempio di un piranosio in quella proiezione.
- Dettagli
- Germán Fernández
- TEORIA DEI CARBOIDRATI
- Visite: 33914
Gli zuccheri in soluzione si trovano principalmente in una forma ciclica, chiamata emiacetale. L'emiacetale si ottiene attaccando uno dei gruppi idrossilici della catena sul carbonile. I cicli formati sono di cinque o sei membri.
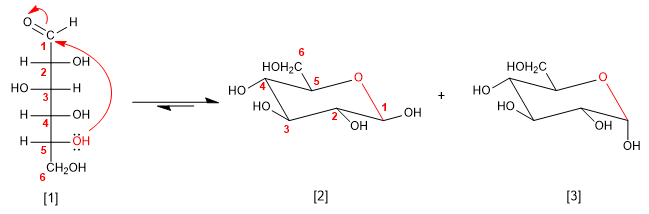
[1] D-Glucosio
[2] b -D-glucopiranosio
[3] a -D-glucopiranosio
- Dettagli
- Germán Fernández
- TEORIA DEI CARBOIDRATI
- Visite: 21475
La mutarotazione è l'interconversione tra anomeri tramite la forma aperta. Pertanto, il glucosio si trova nel mezzo acquoso come una miscela di anomeri alfa e beta e una piccola quantità in forma aperta. Diamo un'occhiata a quell'equilibrio.
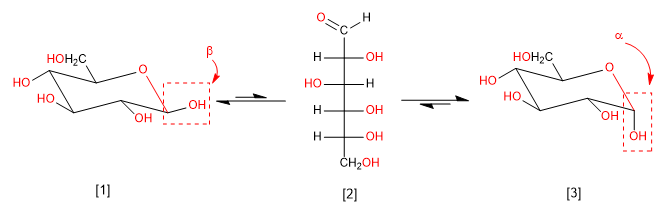
[1] b -D-glucopiranosio (63,6%)
[2] D-Glucosio (0,003%)
[3] a -D-glucopiranosio (36,4%)
- Dettagli
- Germán Fernández
- TEORIA DEI CARBOIDRATI
- Visite: 28614
La sintesi Kiliani-Fischer permette di allungare la catena del monosaccaride attraverso la formazione e la successiva riduzione di cianoidrine. Il grosso problema della sintesi è la mancanza di stereoselettività.
- Dettagli
- Germán Fernández
- TEORIA DEI CARBOIDRATI
- Visite: 16490
Cu(II) e Ag(I) sono in grado di ossidare selettivamente il gruppo carbonilico degli aldosi ad acido carbossilico, generando precipitati di Cu 2 O e Ag elementare.
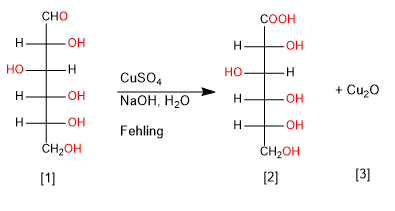
[1] D-Glucosio
[3] Acido D-Gluconico
[4] Precipitato di ossido rameoso