SINTESI DI ALCOLI
(Metodo dell'albero di sintesi)
Proporre un piano di sintesi per le molecole bersaglio indicate dalle singole molecole indicate (MOb 30 -41). Per fare questo, usa i reagenti e le condizioni di reazione che ritieni necessari:
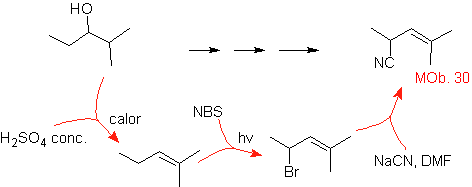
Soluzione MOb 30.
Strategia: si osserva che la molecola di partenza è stata disidratata e nella posizione allilica inizialmente non sostituita, un idrogeno è stato spostato dal gruppo ciano o nitrile. Quest'ultima reazione può avvenire solo se la molecola precursore è un alogenuro allilico, motivo per cui si propone come precursore di
Il Br viene introdotto nella posizione desiderata con l'NBS e l'alchene è il prodotto della disidratazione della molecola di partenza.
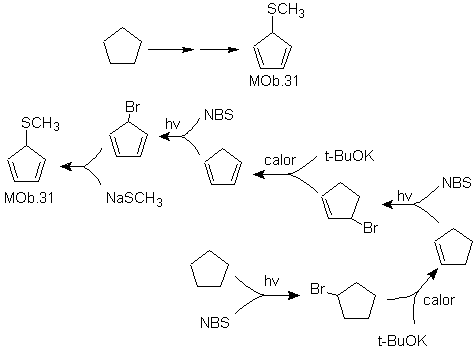
Soluzione MOb 31.
Strategia : è uno zio etere, la molecola precursore necessaria sarà un alogenuro di 1,3-ciclopentadiene.
Questo alogenuro viene preparato per azione dell'NBS sul cicloalchene dienico, che a sua volta viene preparato dalla deidrobromurazione della molecola precursore, che viene raggiunta dall'azione dell'NBS sul cicloalchene formatosi. precedentemente mediante deidroalogenazione della molecola di partenza bromurata dai radicali
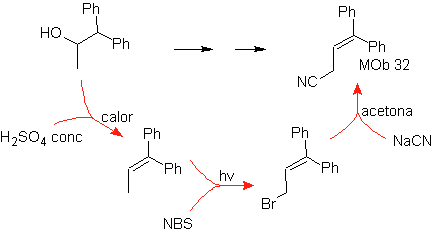
Soluzione Mob 32.
Strategia : è simile a quella utilizzata per ottenere
Soluzione MOb 33.
Strategia :
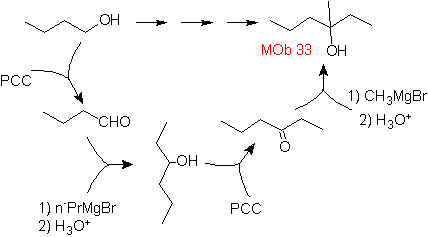
Soluzione MOb 34.
Strategia :
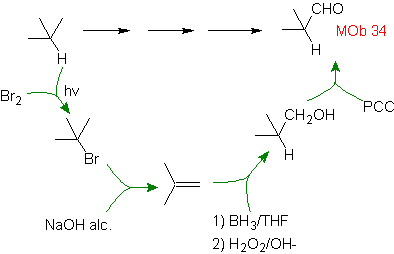
Soluzione MOb 35.
Strategia : viene proposto un alchene come molecola precursore, che viene bromurato in condizioni antimarkovnikov. L'alchene è stato preparato per disidratazione dell'alcool formatosi, per azione di un Grignard su un chetone, che si prepara per ossidazione del cicloesanolo.
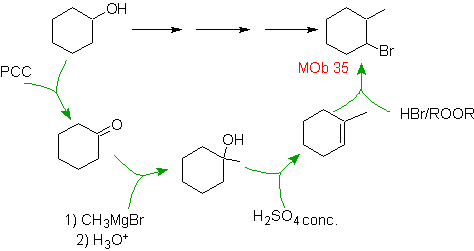
Soluzione MOb 36.
Strategia:
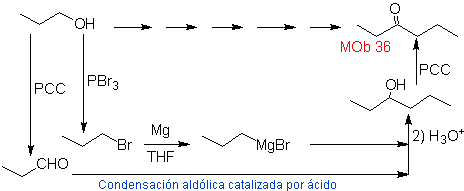
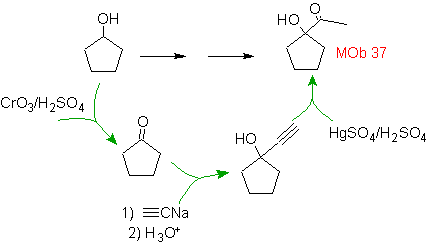
Soluzione MOb 37.
Strategia: Il metilchetone di
L'alcool si è formato per azione dell'acetiluro di sodio su un chetone derivato dall'alcool di partenza per ossidazione.
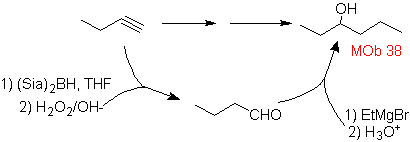
Soluzione mafiosa 38.
Strategia: il materiale di partenza viene ossidato ad aldeide con disiamilborano, che viene attaccato da un adatto Grignard per formare
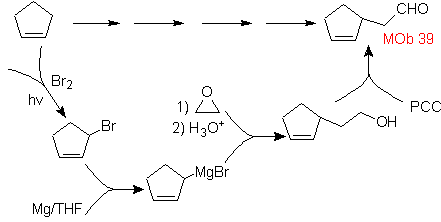
Soluzione mafiosa 39.
Strategia : COME
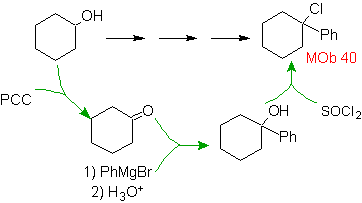
Soluzione MOb 40.
Strategia : gli alogenuri sono ottenuti da alcheni o alcoli, quest'ultima è l'opzione migliore, perché l'azione di un gruppo di Grignard che contiene il gruppo fenile consente la formazione dell'alcol necessario come molecola precursore.
Le due sintesi seguenti richiedono un po' più di impegno da parte del chimico, perché i materiali di partenza definiti richiedono l'uso di alcune reazioni che non sono le più comuni, nonostante le strutture delle molecole bersaglio siano relativamente semplici.
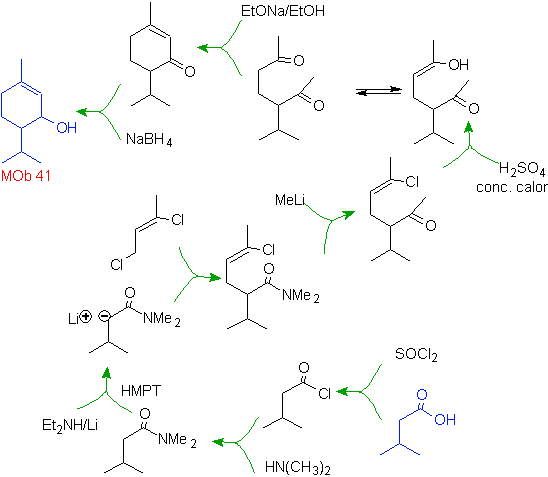
Allora com'è la formazione delle molecole 41 e
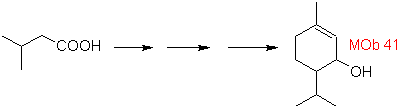
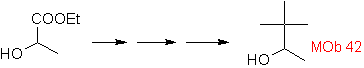
D'altra parte, il metil litio in quantità stechiometriche porta a metil chetone solo quando il substrato è un'ammide o un acido libero (J. Organometal Chem., 9, 165 (1967). In alternativa, si suggerisce anche l'uso di metil magnesio ioduro al posto del metillitio.
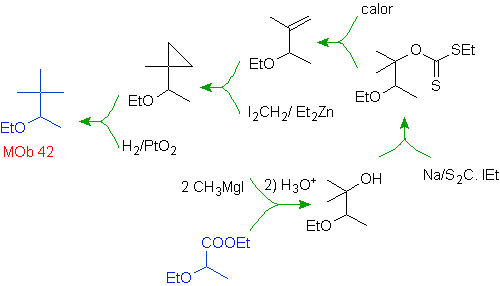
Soluzione Mob 42.
L'apertura della molecola di ciclopropano, un precursore di