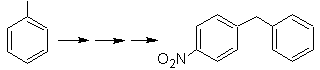SINTESI DI COMPOSTI AROMATICI II
(Metodo dell'albero di sintesi)
Sebbene uno dei primi problemi da risolvere nella sintesi di composti aromatici multisostituiti sia il controllo degli effetti di orientazione e la formazione di isomeri indesiderati, è importante studiare anche la reattività degli areni, poiché ad un certo punto della senso della presenza di gruppi alifatici nel composto aromatico, molte volte, presentano caratteristiche e reattività, tipiche del tipo di composto organico a cui appartengono e quelle particolari che risultano dalla mutua interazione dei gruppi alifatici e aromatici.
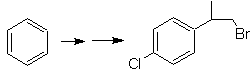
Su questo scopo, si basa, il sintesi delle molecole n. 20 a 27, questa volta da materiali specificati, quindi la domanda è presentata come segue: quali sono le reazioni che Giustificare le seguenti trasformazioni?
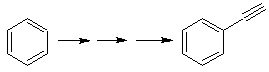
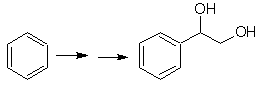
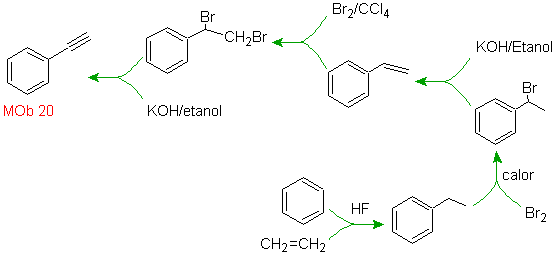
Mob 20 soluzione.
Sappiamo quindi che non esiste alcuna possibilità che lo ione acetiluro agisca direttamente sul benzene il triplo legame è ottenuto da un gruppo alchilico
vec-dibromurato, che si ottiene per bromurazione dello stirene, precedentemente ottenuto per deidrobromurazione di un alogenuro di benzile formato da una bromurazione mediante il meccanismo dei radicali liberi su etilbenzene
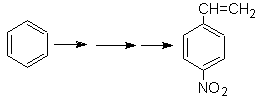
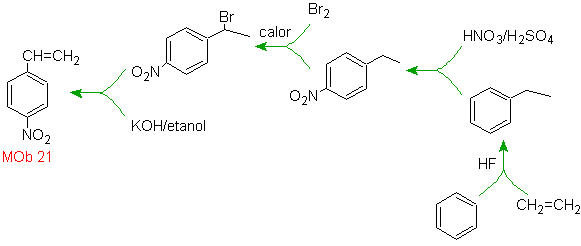
Soluzione Mob 21.
Il paranitrostirene non può essere ottenuto per nitrazione diretta dello stirene, perché il gruppo etenile attaccato all'anello è instabile in condizioni di nitrazione.
Come tale, la molecola precursore avrà un gruppo che è facile da deidrobromurare. Questo precursore si ottiene per bromurazione radicalica del gruppo etilico legato all'anello benzenico, precedentemente nitrato principalmente in posizione para.
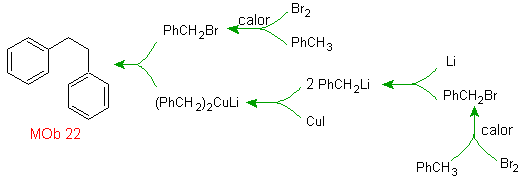
Soluzione MOb 22.
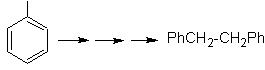
La simmetria della molecola ci permette di pensare a una strategia che tenga conto della reazione di Corey-House. È anche un buon percorso se usi il
PhCH 2 CH 2 Cl, sopra il si tiene conto del benzene o di un'acilazione con PhCH2COCl e successiva riduzione del gruppo carbonilico mediante riduzione di Clemmensen.
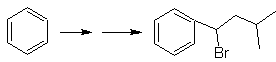
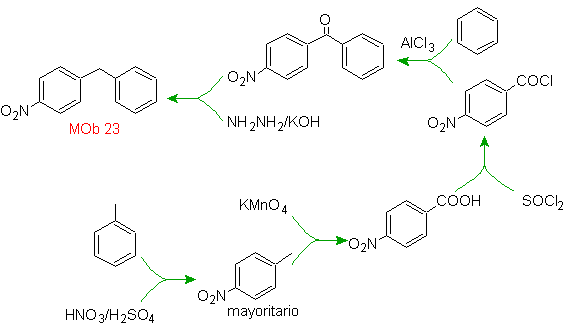
Soluzione mafiosa 23.
La molecola precursore può essere un chetone, il cui gruppo carbonilico è ridotto a metilene dal riducente di Wolf-Kischner. In questo modo si evita la presenza di Zn in ambiente acido che intaccherebbe il gruppo nitro. Un'altra molecola precursore può essere il seguente alogenuro: O 2 N-PhCH 2 Cl che agisce su una molecola di benzene.
La posizione del bromo nella molecola precursore è la tipica posizione allilica, che si ottiene per bromurazione radicalica del corrispondente scheletro carbonioso.
Il gruppo alchilico sull'anello benzenico non può essere ottenuto da alogenuro corrispondente, perché si verificherebbe la trasposizione. Si utilizza quindi l'acilazione e la successiva riduzione del gruppo carbonilico, con amalgamazione dello zinco in ambiente acido (riduzione di Clemmensen
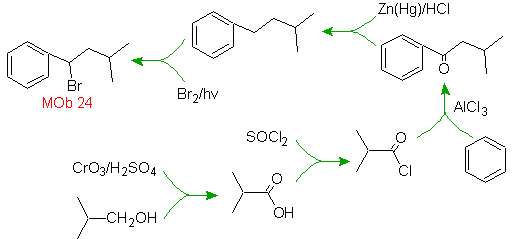
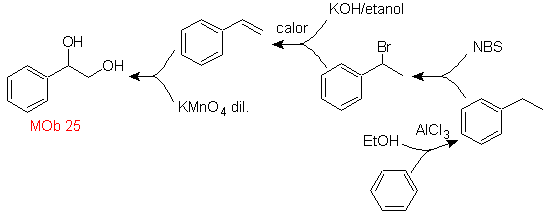
Soluzione MOb 25.
Il diolo di questa molecola può essere ottenuto per idrossilazione selettiva dello stirene, as
molecola precursore. Lo stirene si forma dalla deidrobromurazione, come nei casi precedenti.
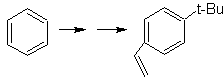
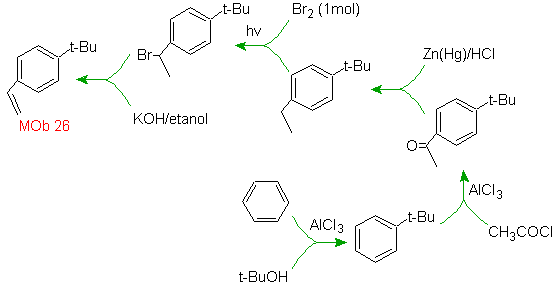
Soluzione MOb 26.
La molecola precursore indica che una possibile via tiene conto della formazione del gruppo etenile da un alogenuro e sfrutta il gruppo voluminoso del t-butile, per introdurre il gruppo acilico che porta il gruppo etilico in posizione para.
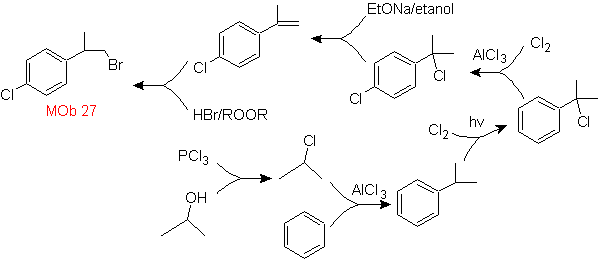
Soluzione mafiosa 27.
La strategia prevede la definizione dell'inclusione del bromuro in una molecola precursore che non consente la formazione di alcun isomero. L'alchene meno sostituito è quello che si forma necessariamente per deidroalogenazione, da un gruppo formato per alogenazione di radicali.
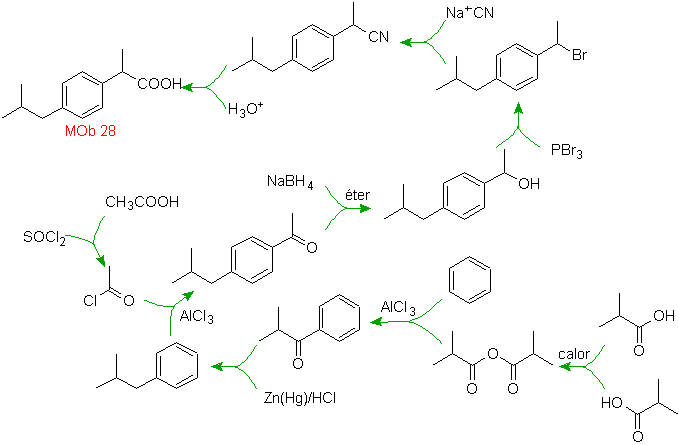
Soluzione MOb 28.
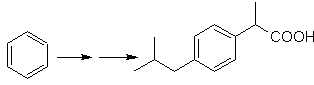
La localizzazione del gruppo carbossilico permette di ipotizzarne la formazione dall'idrolisi del gruppo –CN, quest'ultimo viene introdotto nelle molecole alifatiche generalmente per sostituzione di un alogenuro, che a sua volta deriva da un alcol. Formato dalla riduzione di un chetone carbonile.
Le fasi successive sono legate all'acilazione di Friedel-Crafts, combinata con la riduzione di C=O mediante il metodo di Clemmensen.
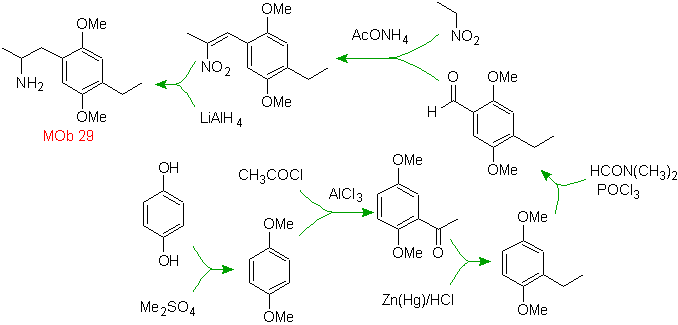
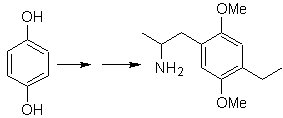
Soluzione MOb 29.
La presenza del gruppo amminico nel residuo alchilico dell'arene, fa pensare al gruppo nitro come suo precursore e per la distanza dall'anello benzenico, si può ipotizzare che sia formato dal nitro - alfa-beta insaturo , risultato della condensazione di tipo aldolico in un mezzo basico con un gruppo –CHO attaccato all'anello benzenico. Questo gruppo formile è inserito nell'anello con una formammide disostituita e ossicloruro di fosforo, nota come reazione di Vilsmeier-Haack. Metodo applicabile solo su substrati aromatici attivati. Per introdurre il gruppo etilico mediante acilazione di Friedel-Crafts, è necessario trasformare preventivamente i gruppi –OH del materiale di partenza in etere metilico.