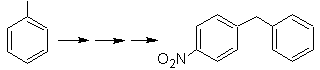SINTESIS SENYAWA AROMATIK II
(Metode Pohon Sintesis)
Meskipun salah satu masalah pertama yang harus diselesaikan dalam sintesis senyawa aromatik multisubstitusi adalah kontrol efek orientasi dan pembentukan isomer yang tidak diinginkan, penting juga untuk mempelajari reaktivitas arena, karena pada beberapa titik di rasa kehadiran gugus alifatik dalam senyawa aromatik, berkali-kali, mereka menunjukkan karakteristik dan reaktivitas, tipikal dari jenis senyawa organik yang mereka miliki dan yang khusus yang dihasilkan dari interaksi timbal balik antara gugus alifatik dan aromatik.
Pada tujuan ini, didasarkan, the sintesis molekul No. 20 hingga 27, kali ini dari bahan yang ditentukan, sehingga pertanyaan yang disajikan sebagai berikut: Apa reaksi itu Benarkan transformasi berikut?
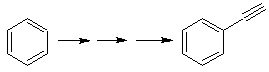
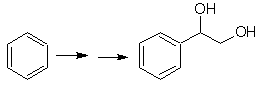
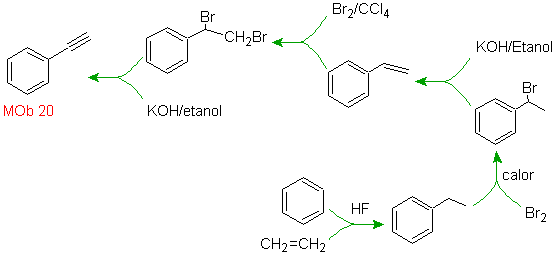
Solusi massa 20.
Kita tahu bahwa tidak ada kemungkinan ion asetilida bekerja langsung pada benzena ikatan rangkap tiga diperoleh dari gugus alkil
vec-dibrominated, yang diperoleh dengan brominating styrene, sebelumnya diperoleh dengan dehydrobrominating dari benzil halida yang dibentuk oleh brominasi oleh mekanisme radikal bebas pada etilbenzena
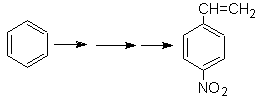
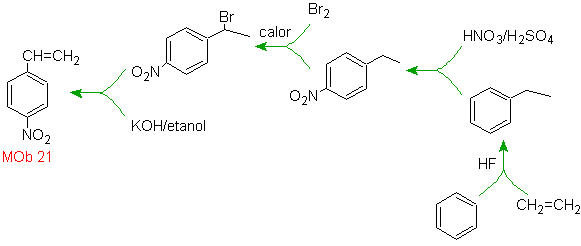
Solusi Massa 21.
Para nitrostirena tidak dapat diperoleh dengan nitrasi langsung dari stirena, karena gugus etenil yang terikat pada cincin tidak stabil dalam kondisi nitrasi.
Dengan demikian, molekul prekursor akan memiliki gugus yang mudah didehidrobrominasi. Prekursor ini diperoleh dengan brominasi radikal dari gugus etil yang berikatan dengan cincin benzena, yang sebelumnya dinitrasi terutama pada posisi para.
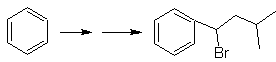
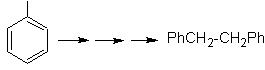
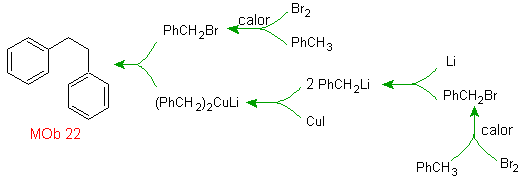
Solusi MOb 22.
Simetri molekul memungkinkan kita memikirkan strategi yang memperhitungkan reaksi Corey-House. Ini juga merupakan rute yang baik jika Anda menggunakan
PhCH 2 CH 2 Cl, di atas benzena atau asilasi dengan PhCH2COCl dan reduksi selanjutnya dari gugus karbonil dengan reduksi Clemmensen diperhitungkan.
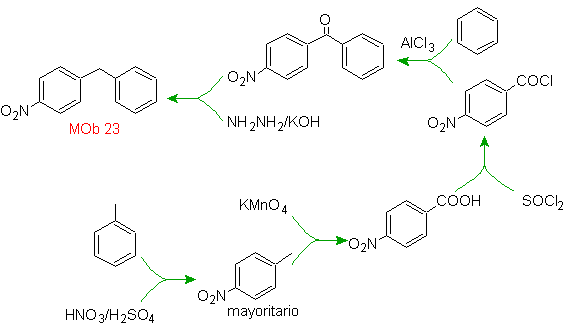
Solusi massa 23.
Molekul prekursor dapat berupa keton, gugus karbonil yang direduksi menjadi metilen oleh reduktor Wolf-Kischner. Dengan cara ini, keberadaan Zn dalam media asam yang akan mempengaruhi gugus nitro dapat dihindari. Molekul prekursor lain dapat berupa halida berikut: O 2 N-PhCH 2 Cl yang bekerja pada molekul benzena.
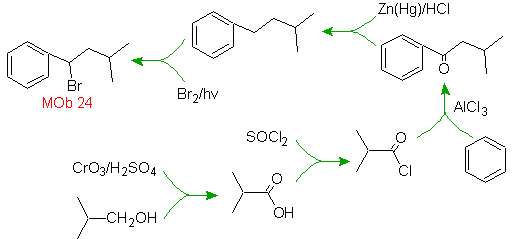
Posisi bromin dalam molekul prekursor adalah posisi alilik yang khas, yang diperoleh dengan brominasi radikal dari kerangka karbon yang sesuai.
Gugus alkil pada cincin benzena tidak dapat diperoleh dari halida yang sesuai, karena transposisi akan terjadi. Kemudian, asilasi dan reduksi selanjutnya dari gugus karbonil digunakan, dengan amalgamasi seng dalam media asam (reduksi Clemmensen
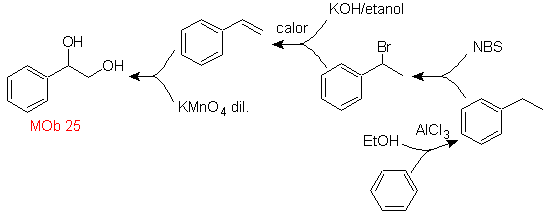
solusi MOb25.
Diol molekul ini dapat diperoleh dengan hidroksilasi selektif stirena, seperti
molekul prekursor. Styrene terbentuk dari dehydrobromination, seperti pada kasus sebelumnya.
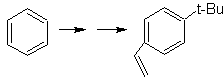
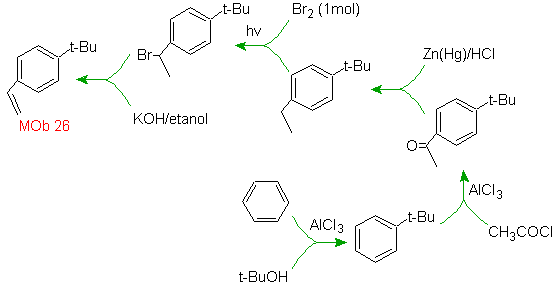
Solusi MOb 26.
Molekul prekursor menunjukkan bahwa rute yang mungkin memperhitungkan pembentukan gugus etenil dari halida dan memanfaatkan gugus t-Butil yang besar, untuk memasukkan gugus asil yang membawa gugus etil pada posisi para.
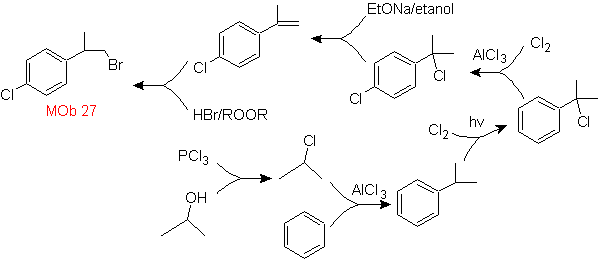
Solusi massa 27.
Strateginya melibatkan penentuan inklusi bromida dalam molekul prekursor yang tidak memungkinkan pembentukan isomer apa pun. Alkena yang paling sedikit tersubstitusi adalah yang harus dibentuk oleh dehidrohalogenasi, dari gugus yang dibentuk oleh radikal Halogenasi.
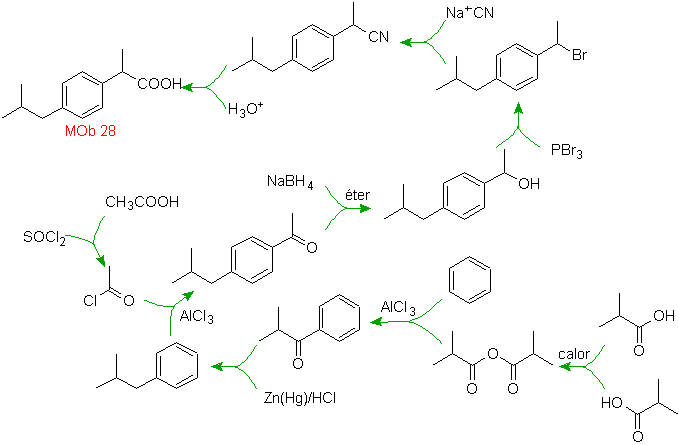
Solusi MOb 28.
Lokasi gugus karboksilat memungkinkan kita untuk mengusulkan pembentukannya dari hidrolisis gugus –CN, yang terakhir dimasukkan ke dalam molekul alifatik umumnya dengan substitusi halida, yang pada gilirannya berasal dari alkohol. Dibentuk dengan reduksi keton karbonil.
Langkah selanjutnya terkait dengan asilasi Friedel-Crafts, digabungkan dengan reduksi C=O dengan metode Clemmensen.
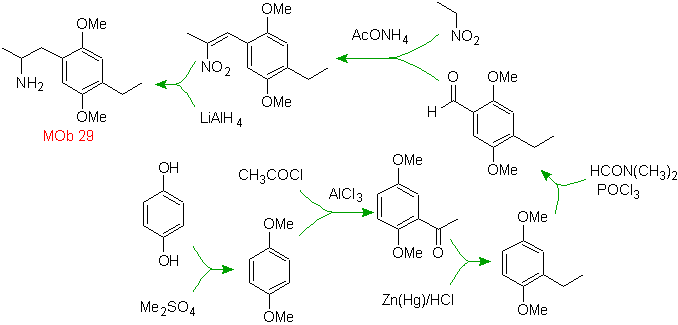
Solusi MOb 29.
Kehadiran gugus amino dalam residu alkil arena, membuat kita menganggap gugus nitro sebagai prekursornya dan karena jaraknya dari cincin benzena, dapat diusulkan bahwa gugus tersebut terbentuk dari gugus tak jenuh nitro - alfa-beta , hasil kondensasi jenis aldol dalam media basa dengan gugus –CHO yang terikat pada cincin benzena. Gugus formil ini dimasukkan ke dalam ring dengan formamida tersubstitusi dan fosfor oksiklorida, dikenal sebagai reaksi Vilsmeier-Haack. Metode yang hanya dapat diterapkan pada substrat aromatik aktif. Untuk memperkenalkan gugus etil dengan Asilasi Friedel-Crafts, sebelumnya perlu mengubah gugus –OH dari bahan awal menjadi metil eter.