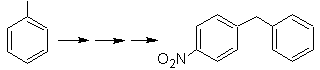СИНТЕЗ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ II
(метод дерева синтеза)
Хотя одной из первых проблем, которые необходимо решить при синтезе полизамещенных ароматических соединений, является контроль ориентационных эффектов и образования нежелательных изомеров, важно также изучить реакционную способность аренов, поскольку в какой-то момент В смысле присутствия алифатических групп в ароматическом соединении они во многих случаях проявляют характеристики и реакционную способность, типичные для типа органического соединения, к которому они принадлежат, и те, которые являются результатом взаимодействия алифатических и ароматических групп.
На этой цели основано, синтез молекул №20-27, на этот раз из указанных материалов, поэтому вопрос ставится так: какие реакции Обоснуйте следующие преобразования?
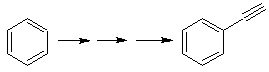
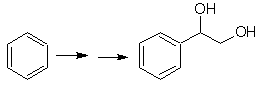
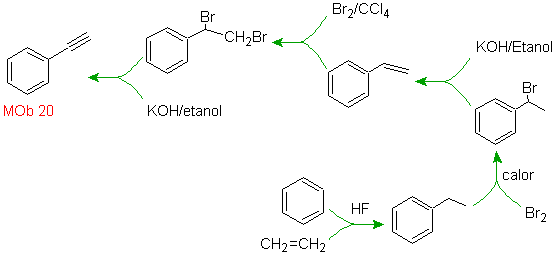
Моб 20 решение.
Мы знаем, что ион ацетилида не может действовать непосредственно на бензол, поэтому тройная связь получается из алкильной группы
век-дибром, который получают бромированием стирола, ранее полученного дегидробромированием бензилгалогенида, образованного бромированием по свободнорадикальному механизму на этилбензоле
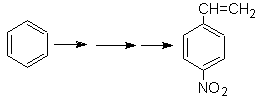
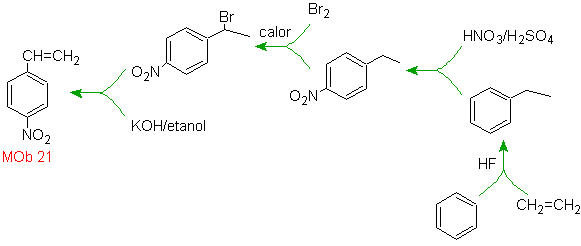
Решение Моб 21.
Пара-нитростирол не может быть получен прямым нитрованием стирола, так как этенильная группа, присоединенная к кольцу, неустойчива в условиях нитрования.
Таким образом, молекула предшественника будет иметь группу, которую легко дегидробромировать. Этот предшественник получают радикальным бромированием этильной группы, связанной с бензольным кольцом, которое ранее нитровали преимущественно в пара-положении.
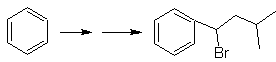
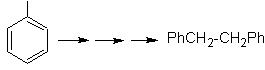
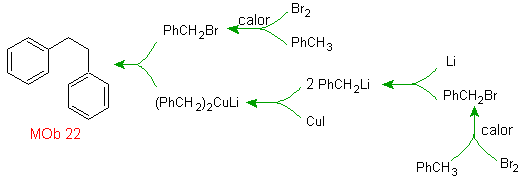
Решение МОБ 22.
Симметрия молекулы позволяет нам думать о стратегии, учитывающей реакцию Кори-Хауза. Это также хороший маршрут, если вы используете
PhCH 2 CH 2 Cl, над бензолом или ацилированием PhCH2COCl и последующим восстановлением карбонильной группы методом Клемменсена.
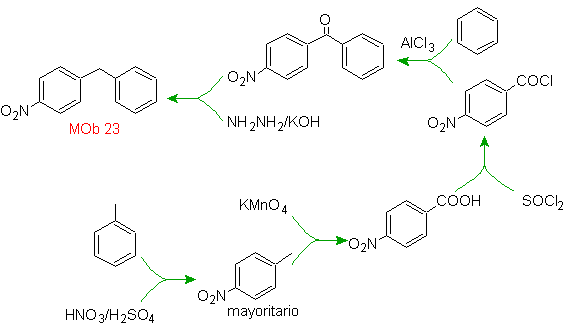
Моб раствор 23.
Молекула-предшественник может представлять собой кетон, карбонильная группа которого восстанавливается до метилена восстановителем Вольфа-Кишнера. Таким образом, предотвращается присутствие Zn в кислой среде, которое могло бы воздействовать на нитрогруппу. Другой молекулой-предшественником может быть следующий галогенид: O 2 N-PhCH 2 Cl, который действует на молекулу бензола.
Положение брома в молекуле предшественника является типичным аллильным положением, которое получается радикальным бромированием соответствующего углеродного скелета.
Алкильная группа бензольного кольца не может быть получена из соответствующий галогенид, потому что произойдет транспозиция. Затем применяют ацилирование и последующее восстановление карбонильной группы с амальгамированием цинка в кислой среде (восстановление Клемменсена).
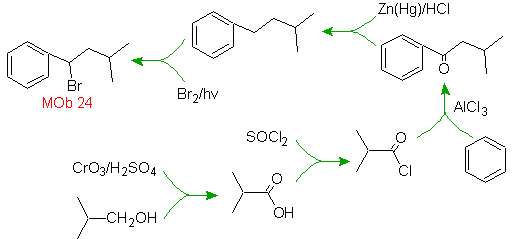
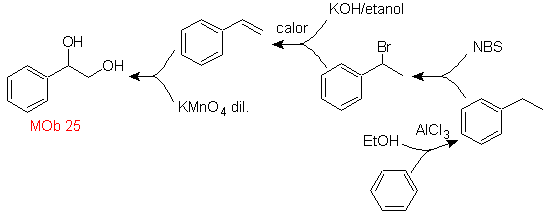
раствор МОБ 25.
Диол этой молекулы может быть получен селективным гидроксилированием стирола, т.к.
молекула-предшественник. Стирол образуется в результате дегидробромирования, как и в предыдущих случаях.
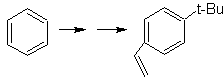
Решение МОБ 26.
Молекула предшественника указывает на то, что возможный путь учитывает образование этенильной группы из галогенида и использует объемистую группу трет-бутила для введения ацильной группы, несущей этильную группу в пара-положении.
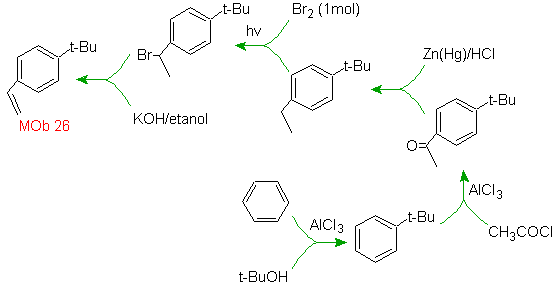
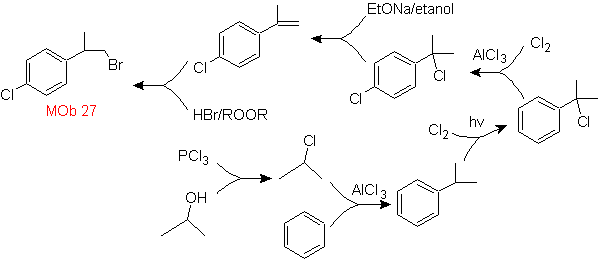
Моб раствор 27.
Стратегия включает в себя определение включения бромида в молекулу предшественника, которое не допускает образования какого-либо изомера. Наименее замещенным алкеном является тот, который обязательно образуется в результате дегидрогалогенирования из группы, образованной в результате галогенирования радикалов.
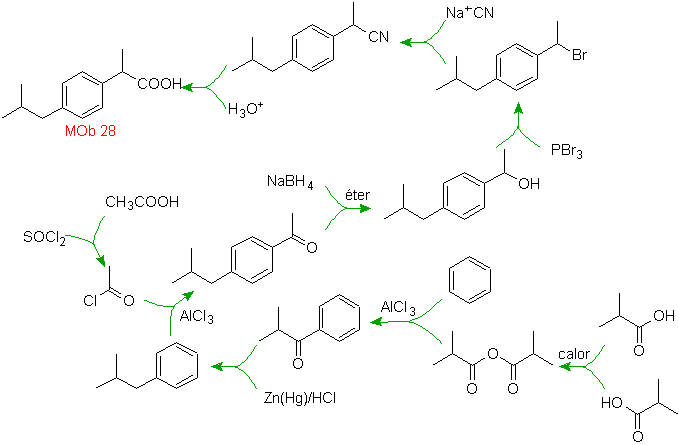
Решение МОБ 28.
Расположение карбоксильной группы позволяет предположить ее образование в результате гидролиза группы –CN, последняя вводится в алифатические молекулы, как правило, путем замещения галогенида, который, в свою очередь, происходит от спирта. Образуется путем восстановления карбонила кетона.
Последующие стадии связаны с ацилированием Фриделя-Крафтса в сочетании с восстановлением C=O по методу Клемменсена.
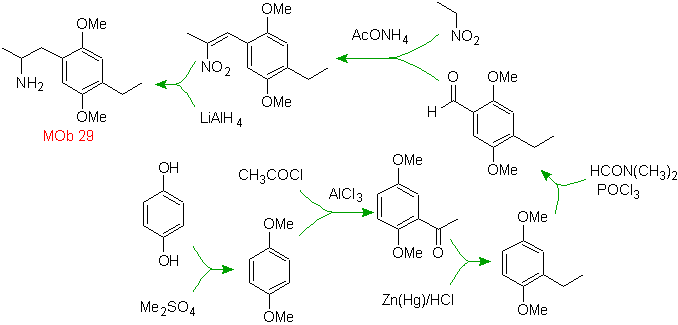
Решение МОБ 29.
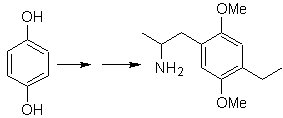
Наличие аминогруппы в алкильном остатке арена заставляет думать о нитрогруппе как о его предшественнике и ввиду удаленности от бензольного кольца можно предположить, что она образована из нитро-альфа-бета-ненасыщенного , результат конденсации альдольного типа в основной среде с присоединенной к бензольному кольцу группой –CHO. Эта формильная группа вставлена в кольцо с дизамещенным формамидом и оксихлоридом фосфора, известной как реакция Вильсмейера-Хаака. Метод, применимый только к активированным ароматическим субстратам. Чтобы ввести этильную группу ацилированием Фриделя-Крафтса, необходимо предварительно преобразовать группы –ОН исходного вещества в метиловый эфир.