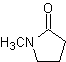
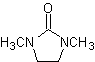
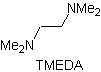
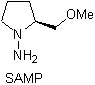
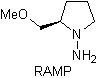
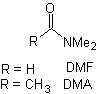Reazioni di enoli ed enolati
Reazioni aldoliche e cosiddette reazioni di condensazione di composti carbonilici e altre di questo tipo, che possono formare strutture enoliche ed enolate, partecipano a un ampio gruppo di reazioni importanti che ci permettono di comprendere l'esistenza di un numero immenso di molecole risultanti dall'interazione di enoli o enolati con una serie di gruppi elettrofili.
Lo studio di questo tipo di reazioni ha permesso di verificare e stabilire l'esistenza di due meccanismi di reazione attraverso i quali si verificano, come spiegato di seguito:
A)
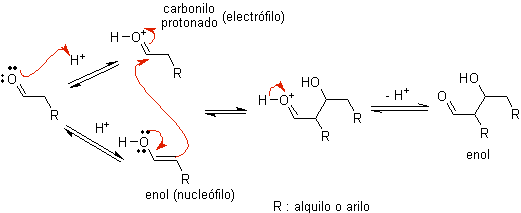
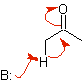
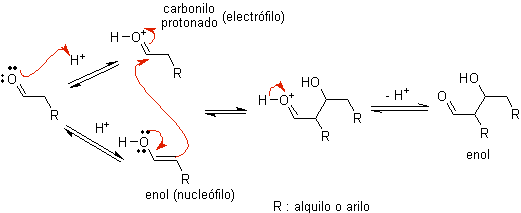
Quando l'acido viene utilizzato come catalizzatore, il composto carbonilico viene inizialmente protonato e quindi tautomerizzato nella sua forma enolica , che è un nucleofilo sul carbonio alfa del gruppo carbonilico. Lo stesso mezzo acido è sufficiente per attivare il gruppo carbonilico di un'altra molecola, rendendolo altamente elettrofilo, che genera condizioni ottimali per produrre un composto carbonilico insaturo.
La reazione procede normalmente fino alla disidratazione dell'enolo formatosi, catalizzata dallo stesso acido della reazione.
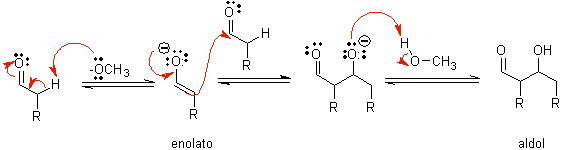
B) Quando il catalizzatore è una base, come un alcossido, la reazione di tipo aldolico procede attraverso l'attacco nucleofilo dell'enolato stabilizzato per risonanza sul gruppo carbonilico di un'altra molecola.
Per disidratazione dell'aldolo, catalizzata dalla base, si forma il prodotto finale disidratato.
Come nel caso precedente, la disidratazione base-catalizzata (a volte scritta come un singolo passaggio), permette di controllare la reazione e produrre un prodotto finale disidratato. In alcuni casi, la formazione di enolati è irreversibile.
come appare in alcuni casi è richiesta solo una quantità catalitica di base, la procedura più comune consiste nell'utilizzare una quantità estequiométrica di base forte comeLDA o NaHMDS . In questo caso, la formazione dell'enolato è irreversibile e il prodotto aldolico non si forma finché l'alcossido metallico del prodotto aldolico non viene protonato in una fase successiva.
Equivalenti sintetici di vari enoli ed enolati
enolato |
azaenolato |
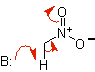
enolato di nitroalcano |
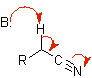
enolato di nitrile |
| |||
estere, ammide |
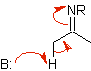
immina |
nitroalcano |
nitrile |
enolo |
enolo etere |
enolo estere |
Silil enol etere |
enamine |
Alchilazione di enoli ed enolati:
L'alchilazione degli enolati corrisponde principalmente a una reazione di sostituzione nucleofila con alogenuri alchilici ed epossidi. In questa reazione, gli alogenuri alchilici primari e benzilici sono buoni per l'alchilazione, gli alogenuri alchilici secondari solo in alcuni casi e gli alogenuri alchilici terziari sostanzialmente non reagiscono con gli enolati, perché la reazione procede mediante un meccanismo di sostituzione nucleofila.
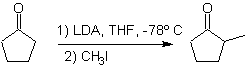
D'altra parte, la velocità dell'alchilazione è aumentata dalla polarità dei solventi utilizzati come mezzo di reazione.
|
|
| ||
|
|
| ||
TORCIA | NaHMDS | DIPEA | ||
Cy2BCl | Bu 2 BOTF |
Alchilazione di silil enol eteri , catalizzata da acidi di Lewis. Alchilazione Y N 1


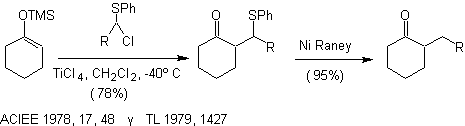
Alchilazione di enolati di composti a , b carbonili insaturi:
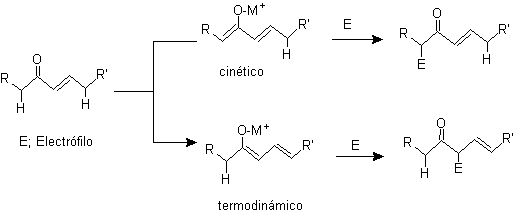
¨
g -alchilazione di chetoni insaturi in a , b
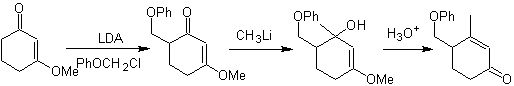
Alchilazione delle enammine .
La monolaquilazione e la formazione del prodotto cinetico sono controllate, sfruttando l'effetto sterico, per il quale deve essere utilizzata un'ammina secondaria voluminosa come la morfolina.
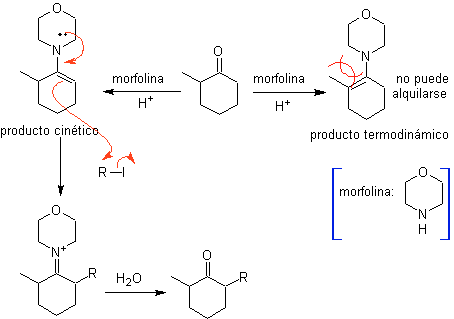
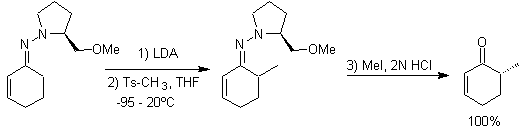
D'altra parte, le enammine chirali , producono in alchilazione anche chetoni alfa sostituiti chirali
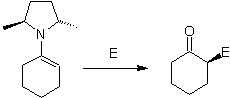
Alchil immine: le immine, che sono isoelettroniche con i chetoni, possono essere trasformate in enammine, che possono quindi essere alchilate o fatte reagire con un reagente. elettrofilo.
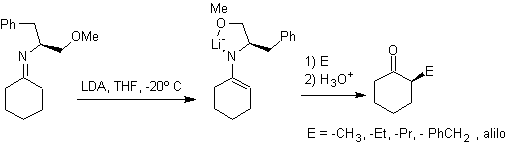
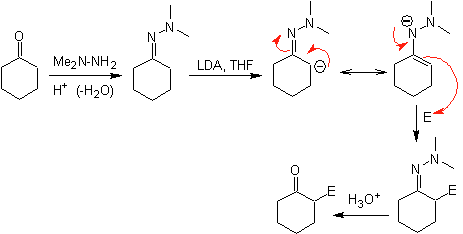
¨
Gli anioni idrazone sono molto più reattivi dei corrispondenti enolati aldeidici o chetonici.
¨
C'è un inconveniente, poiché potrebbero esserci difficoltà nell'idrolisi finale.
¨
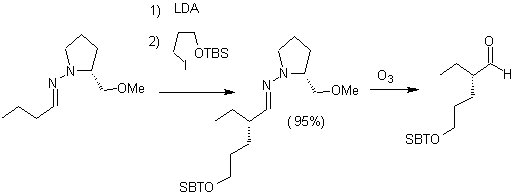
Gli idrazoni chirali sono usati per l'alchilazione asimmetrica (gli idrazoni RAMP/SAMP sono usati nella sintesi asimmetrica)
|
|