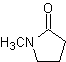
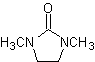
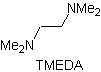
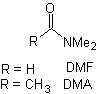Реакции енолов и енолятов
Альдольные реакции и так называемые реакции конденсации карбонильных соединений и др. этого типа, способные образовывать енольную и енолятную структуры, участвуют в большой группе важных реакций, позволяющих понять существование огромного числа молекул, образующихся в результате взаимодействия енолов или енолятов с рядом электрофильных групп.
Изучение этого типа реакций позволило проверить и установить существование двух механизмов реакции, посредством которых они протекают, как поясняется ниже:
К)
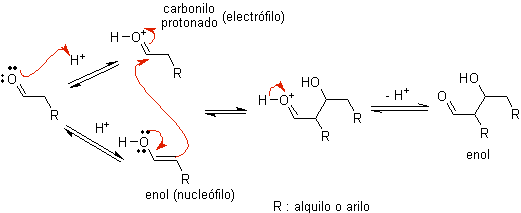
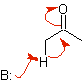
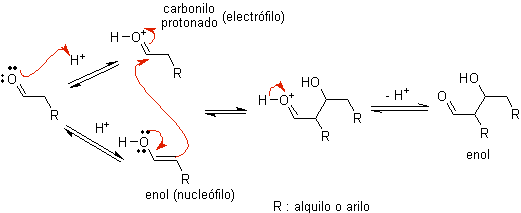
Когда в качестве катализатора используется кислота , карбонильное соединение сначала протонируется, а затем таутомеризуется до его енольной формы , которая является нуклеофилом на альфа-углероде по отношению к карбонильной группе. Той же кислой среды достаточно, чтобы активировать карбонильную группу другой молекулы, делая ее высокоэлектрофильной, что создает оптимальные условия для образования ненасыщенного карбонильного соединения.
Реакция обычно протекает до тех пор, пока не образуется дегидратация енола, катализируемая той же кислотой реакции.
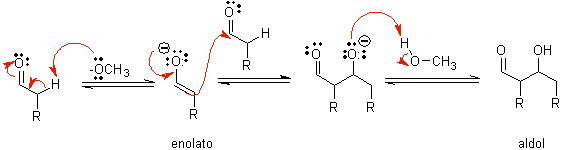
Б) Когда катализатор представляет собой основание, такое как алкоксид, реакция альдольного типа протекает посредством нуклеофильной атаки резонансно-стабилизированного енолята на карбонильную группу другой молекулы.
При дегидратации альдола, катализируемой основанием, образуется обезвоженный конечный продукт.
Как и в предыдущем случае, дегидратация, катализируемая основанием (иногда описываемая как одностадийная), позволяет контролировать реакцию и получать дегидратированный конечный продукт. В некоторых случаях образование енолятов носит необратимый характер.
как это выглядит в некоторых случаях требуется только каталитическое количество основания, наиболее обычная процедура заключается в использовании estequiométrica количества сильного основания, такого как LDA или NaHMDS . В этом случае образование енолята является необратимым, и альдольный продукт не образуется до тех пор, пока алкоксид металла альдольного продукта не будет протонирован на более поздней стадии.
Синтетические эквиваленты различных енолов и енолятов
енолят |
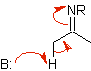
азаенолат |
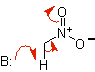
енолят нитроалкана |
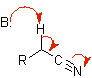
енолят нитрила |
| |||
сложный эфир, амид |
я добываю |
нитроалкан |
Нитрил |
енол |
еноловый эфир |
энольный эфир |
силиленоловый эфир |
энамин |
Алкилирование енолов и енолятов:
Алкилирование енолятов в основном соответствует реакции нуклеофильного замещения с алкилгалогенидами и эпоксидами. В этой реакции первичные алкилгалогениды и бензилгалогениды хороши для алкилирования, вторичные алкилгалогениды лишь в некоторых случаях, а третичные алкилгалогениды в основном не реагируют с енолятами, так как реакция протекает по механизму нуклеофильного замещения.
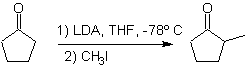
С другой стороны, скорость алкилирования увеличивается за счет полярности растворителей, используемых в качестве реакционной среды.
|
|
| ||
|
|
| ||
ФАКЕЛ | NaHMDS | ДИПЕА | ||
Cy2BCl | Бу 2 БОТФ |
Алкилирование эфиров силиленола , катализируемое кислотами Льюиса. Алкилирование Y N 1


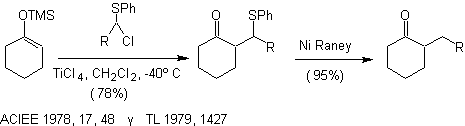
Алкилирование енолятов соединений а , б ненасыщенные карбонилы:
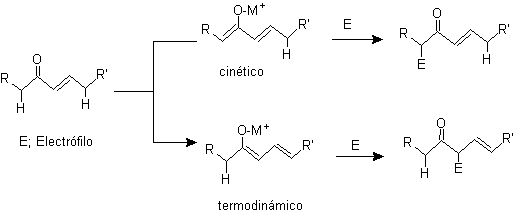
¨
г -алкилирование ненасыщенных кетонов в а , б
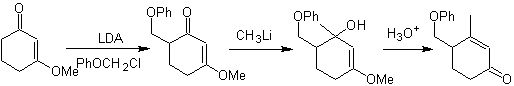
Алкилирование енаминов .
Монолакилирование и образование кинетического продукта контролируются за счет стерического эффекта, для которого необходимо использовать объемный вторичный амин, такой как морфолин.
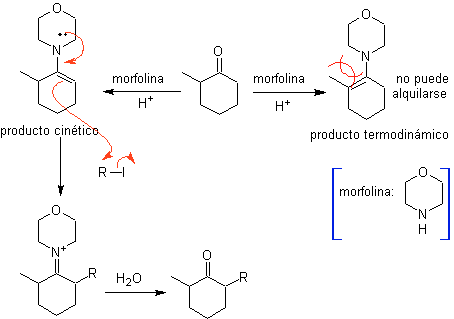
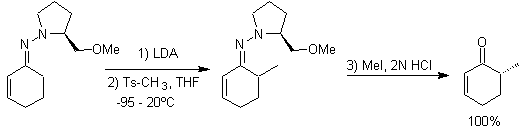
С другой стороны, хиральные енамины при алкилировании дают также хиральные альфа-замещенные кетоны.
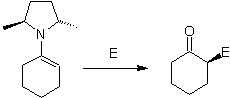
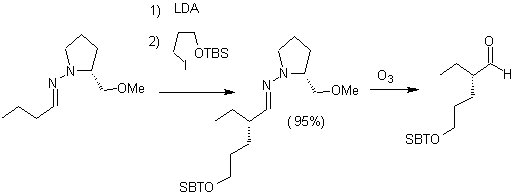
Алкилимины: Имины, которые изоэлектронны кетонам, могут быть преобразованы в енамины, которые затем могут быть алкилированы или подвергнуты реакции с реагентом. электрофил.
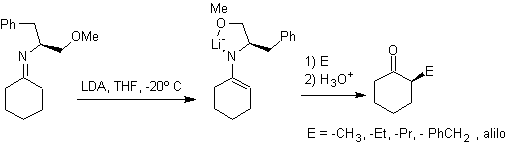
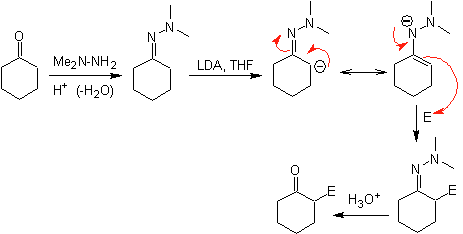
¨
Анионы гидразона гораздо более реакционноспособны, чем соответствующие еноляты альдегидов или кетонов.
¨
Есть недостаток, так как могут возникнуть трудности при окончательном гидролизе.
¨
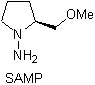
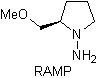
Хиральные гидразоны используются для асимметричного алкилирования (гидразоны RAMP / SAMP используются в асимметричном синтезе).
|
|