Cyclisation intramoléculaire (Williamson intramoléculaire) : Les alcools halogénés en position 2 se cyclisent en milieu basique pour former des oxiranes.
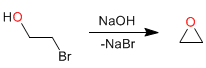
Mécanisme:
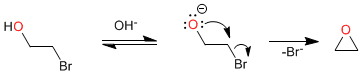
La première étape du mécanisme consiste en un équilibre acido-basique qui dépotifie l'alcool, générant un bon nucléophile (alcoxyde) qui se cyclise dans la deuxième étape par un S N 2 intramoléculaire.
Époxydation d'alcène : Les peracides (MCPBA) réagissent avec les alcènes pour former des oxiranes (époxydes).

Mécanisme:
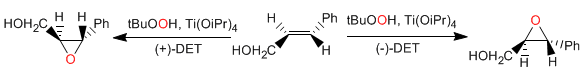
Époxydation asymétrique de Sharples : les alcools allyliques réagissent de manière énantiosélective avec le tétraisopropoxyde de titane, l'hydroperoxyde de tert-butyle et le tartrate de diéthyle (+) ou (-) pour donner des oxiranes.
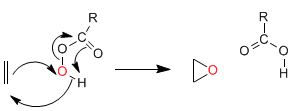
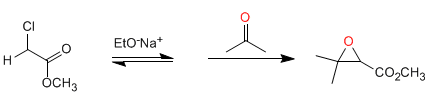
Synthèse de Darzens : La réaction démarre à partir d'esters halogénés en position alpha, qui forment des énolates en milieu basique. La réaction de l'ester d'énolate avec des aldéhydes ou des cétones, suivie de S N 2 intramoléculaire, produit des oxiranes.
Mécanisme:
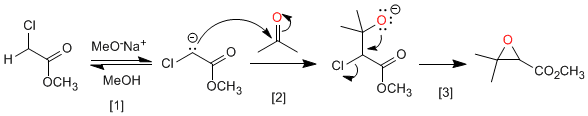
[1] Déprotonation d'ester.
[2] Attaque nucléophile de l'ester d'énolate sur le carbonyle.
[3 ] Substitution nucléophile intramoléculaire qui génère de l'oxirane.
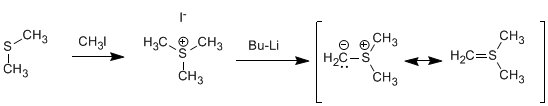
Synthèse Corey (ylures de soufre) : Les ylures de soufre réagissent avec les aldéhydes ou les cétones pour former des oxiranes.
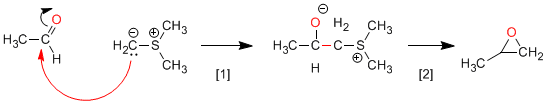
[1] Attaque nucléophile de l'ylure au carbonyle.
[2 ] Étape de cyclisation tirant parti de la capacité du soufre comme groupe partant.
L'ylure de soufre est préparé par méthylation du sulfure de diméthyle suivi d'un traitement avec une base forte.