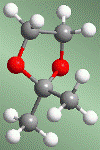
 Les acétals peuvent être utilisés, en raison de leur stabilité, comme groupes protecteurs carbonyle. L'acétal est un éther, très stable en milieu basique, bien qu'il se brise en présence de milieu acide. Dans de nombreux procédés de synthèse, le groupement carbonyle est incompatible avec le réactif utilisé. Dans ces cas, il doit être protégé pour l'empêcher de réagir. L'instabilité de l'acétal en milieu acide peut être utilisée pour déprotéger le carbonyle.
Les acétals peuvent être utilisés, en raison de leur stabilité, comme groupes protecteurs carbonyle. L'acétal est un éther, très stable en milieu basique, bien qu'il se brise en présence de milieu acide. Dans de nombreux procédés de synthèse, le groupement carbonyle est incompatible avec le réactif utilisé. Dans ces cas, il doit être protégé pour l'empêcher de réagir. L'instabilité de l'acétal en milieu acide peut être utilisée pour déprotéger le carbonyle.
Voyons quelques exemples :
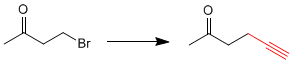
Cette transformation nécessite une substitution, utilisant l'acétylure de sodium comme nucléophile. Le nucléophile peut aussi attaquer le groupe carbonyle, pour l'éviter on va le protéger.
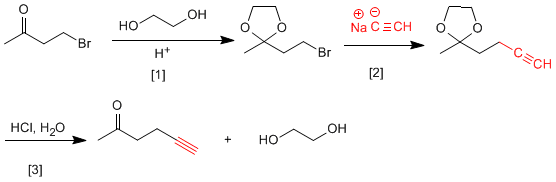
[1] Protection cétonique.
[2] Attaque de l'acétylure sur le carbone brome.
[3] Déprotection du carbonyle
Prenons un deuxième exemple :
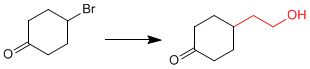
Il est nécessaire de protéger la cétone avant de former l'organométallique pour éviter la dimérisation du composé.
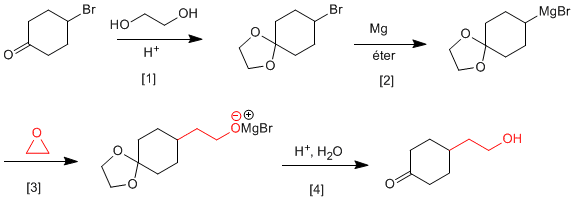
[1] Protection cétonique.
[2 ] Formation magnésienne.
[3] Ouverture de l'oxacyclopropane.
[4] Déprotection et protonation de l'alcoolate.